Антибиотикорезистентность - фактор, определяющий выбор антимикробных препаратов для терапии инфекций мочевыводящих путей
Л.С. Страчунский В.В. Рафальский
НИИ антимикробной терапии Смоленской государственной медицинской академииВыбор препарата для лечения пациентов с внебольничными инфекциями мочевыводящих путей (ИМП) традиционно базируется на 2 основополагающих положениях. Первое заключается в том, что структура возбудителей, вызывающих амбулаторные ИМП, с высокой долей вероятности предсказуема: 75-90% случаев инфекции вызывает Escherichia coli, 5-10% - Staphylococcus saprophyticus и 5-10% - другие возбудители [1]. Второе положение подразумевает необходимость принимать во внимание резистентность этих возбудителей, в первую очередь E. coli. Исходя из этих положений, эмпирическая терапия короткими курсами ко-тримоксазола, до последнего времени являлась терапией выбора острого цистита в большинстве стран мира [2]. Приведенные выше положения, применимы и при эмпирическом выборе начальной терапии острого пиелонефрита и осложненных ИМП. Как правило, в дальнейшем, антибиотикотерапия этих форм ИМП может корректироваться после получения результатов бактериологического исследования мочи.
Антибиотикорезистентность, которая традиционно считалась проблемой только для внутрибольничных инфекций и осложненных ИМП, выходит сейчас на первый план при неосложненных амбулаторных ИМП. В течение последних десятилетий в мире отмечено несколько тенденций в динамике антибиотикорезистентности уропатогенной E. coli, заставляющих пересматривать требования к антибиотикам для терапии ИМП. В частности, наиболее авторитетными руководствами по терапии ИМП, не рекомендуется использовать ко-тримоксазол, как препарат выбора, при неосложненных ИМП, если уровень резистентности E.coli к этому антибиотику превышает 10-20% [2, 6]. В регионах, где уровень резистентности к ко-тримоксазолу превышает пороговый уровень, в качестве препаратов выбора должны рассматриваться другие антимикробные препараты, такие как фторхинолоны, фосфомицин.
Этиология внебольничных ИМП
Существует два важных фактора влияющих на особенности этиологии и резистентности возбудителей ИМП - место возникновения инфекции и наличие осложняющих факторов. По месту возникновения ИМП принято подразделять на внебольничные (амбулаторные) и госпитальные (нозокомиальные, внутрибольничные). Первые возникают у амбулаторных пациентов вне стационаров, хотя могут быть причиной госпитализации. К госпитальным ИМП относят инфекции, развившиеся не ранее 48 после госпитализации пациентов в стационар. Этиология внебольничных ИМП достаточно хорошо изучена за последние десятилетия. Главной особенностью этих инфекций является достаточно прогнозируемый спектр возбудителей, на 85-95% представленный бактериями рода Enterobacteriacea, в основном E.coli. Структура возбудителей нозокомиальных ИМП существенно сложнее - доля E.coli как правило значительно ниже, возрастает роль P.auroginosa, неферментирующих грамотрицательных палочек, энтерококков, стафилококков. Спектр возбудителей нозокомиальных ИМП достаточно сложно предсказать, так как он может значительно отличаться между разными городами, стационарами и даже между разными отделениями одного и того же стационара. В рамках настоящей статьи будут обсуждаться особенности этиологии и резистентности только амбулаторных ИМП.
Наличие или отсутствие осложняющих факторов у пациентов с ИМП является одним из ключевых параметров, определяющих особенности наблюдения пациентов и выбора терапии [28]. К микробиологическим особенностям осложненных ИМП относятся: более широкий спектр возбудителей и высокая частота выделения резистентных бактерий, по сравнению с неосложненными ИМП [29]. E. coli является основным возбудителем как при неосложненных, так и при осложненных ИМП. Однако, при осложненных ИМП более часто выделяются другие бактерии, такие как, Proteus mirabilis, Klebsiella spp., Citrobacter spp., Pseudomonas spp., Enterococcus spp. и др.
Полученные нами данные свидетельствуют о том, что основным возбудителем внебольничных ИМП в России у всех категорий пациентов является E. coli [30]. Наибольшее этиологическое значение E.coli имеет при внебольничных ИМП у взрослых пациентов (85,9%) и несколько меньше у беременных женщин и детей (53,1% и 62,9% соответственно). Учитывая наибольшую этиологическую значимость E.сoli в структуре ИМП во всех изучаемых популяциях пациентов, для практики, в первую очередь, важно знать антибиотикорезистентность именно этого возбудителя.
Антибиотикорезистентность E.сoli
Мониторинг резистентности возбудителей ИМП постоянно проводятся во многих странах мира, и является либо самостоятельным исследованием, либо частью более масштабных проектов, например SENTRY. Нередко эти исследования являются многоцентровыми международными, например проект ECO-SENS, который проводится на территории стран Европы и Канады [8].
Для анализа изменений резистентности уропатогенов к антибиотикам с течением времени наибольший интерес представляют эпидемиологические исследования, проводимые в Северной Америке в течение последних 10-15 лет [7, 14] (Рисунок 1). В США, как и большинстве стран Европы, отмечается четкая тенденция роста резистентности уропатогенной E.coli к аминопенициллинам (ампициллин) и ко-тримоксазолу. В то же время чувствительность к нитрофурантоину и фторхинолонам (ципрофлоксацин) остается высокой. Данные исследования ECO-SENS свидетельствуют о высоком уровне устойчивости в Европе уропатогенной E.coli к таким антибиотикам как ампициллин и ко-тримоксазол. Резистентность к фторхинолонам, нитрофуранам и фосфомицину по данным этого исследования была невысокой.
Рисунок 1. Динамика резистентности штаммов E.coli, выделенных у взрослых с неосложненными внебольничными ИМП в Северной Америке, % [7]
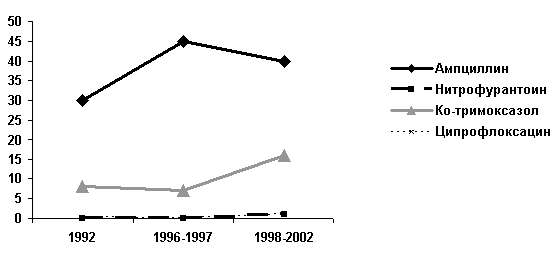
Исследование ECO-SENS подтвердило предположение о существовании значительных географических отличий в уровне и характере антибиотикорезистентности. Так, частота выделения штаммов E.coli, резистентных к ко-тримоксазолу, колебалась от 12,2% в Великобритании до 25,7% в Испании, а к ципрофлоксацину от 0,6% до 14,7% в тех же странах.
Таблица 1. Резистентности штаммов E.coli, выделенных у взрослых с неосложненными внебольничными ИМП в некоторых странах Европы, данные исследования ECO-SENS, % [8]
Страна Ампициллин Ко-тримоксазол Ципрофлоксацин Нитрофурантоин Фосфомицин Бельгия 30,7 14,6 2,9 0,7 0,7 Франция 27,6 15,1 2,0 1,0 1,0 Германия 29 21 2,2 0,7 0 Нидерланды 28,7 10,3 2,1 1,0 0,5 Норвегия 23,8 11,3 0 0 1,2 Испания 53,9 25,7 14,7 4,2 0,5 Великобритания 37,2 12,2 0,6 0 0 По всем странам в среднем 29,8 14,8 2,3 1,2 0,7 В связи с существованием региональных отличий в уровне антибиотикорезистентности, крайне важной задачей является мониторинг резистентности возбудителей ИМП в России. Данные по этиологии возбудителей различных форм амбулаторных ИМП и их антибиотикорезистености были получены в ходе многоцентровых проспективных эпидемиологических исследований UTIAP-I, UTIAP-II, АРМИД, АРИМБ, организованных НИИ антимикробной химиотерапии Смоленской государственной медицинской академии и Научно-методическим центром по мониторингу за антибиотикорезистентностью Минздрава России. Особенностью данных исследований явилось использование во всех исследовательских центрах стандартизованной методики бактериологического исследования мочи. Собранные в исследовательских центрах штаммы передавались для реидентификации и определения чувствительности к антибактериальным препаратам в центральную лабораторию. Оценка чувствительности микроорганизмов была проведена к основным антибиотикам применяемых для терапии ИМП: ампициллину, амоксициллину/клавуланату, гентамицину, ко-тримоксазолу, нитрофурантоину, цефуроксиму, цефотаксиму, ципрофлоксацину, фосфомицину.
При анализе данных по устойчивости у всех категорий пациентов с амбулаторными ИМП (взрослые, беременные женщины, дети), были выявлены сходные закономерности (Таблица 2). Наиболее активным препаратом во всех популяциях пациентов с внебольничными ИМП явился фосфомицин - не выявлено ни одного резистентного к данному антибиотику штамма E.coli. Также достаточно высокой активностью обладали ко-амоксиклав, цефалоспорины II-III, фторхинолоны. Наиболее высокий уровень резистентности уропатогенной E.coli определялся к таким антибиотикам как ампициллин (амоксициллин) - частота выявления устойчивых штаммов от 31,6 до 51,5% и ко-тримоксазолу от 14,5 % до 35,5%.
Таблица 2. Резистентность E.coli, выделенной у пациентов с амбулаторными ИМП в России, к пероральным антибиотикам, %
Антибиотик Категория пациентов Беременные с ИМП, n=117 ИМП у взрослых, n=428 ИМП у детей, n=330 Ампициллин (амоксициллин) 31,6 37,1 51,5 Амоксициллин/клавуланат 3,4 2,6 3,9 Цефуроксим 3,4 2,4 3,9 Ко-тримоксазол 14,5 21 35,5 Нитрофурантоин 4,3 1,2 - Налидиксовая к-та - 6,9 7 Ципрофлоксацин - 4,3 - Фосфомицин 0 0 0 Нитроксолин - 92,91 -
1 - частота выделения нечувствительных штаммов (резистентные+умереннорезистентные)β-лактамы
Высокая резистентность возбудителей ИМП к β-лактамам описана в литературе достаточно давно. Около 25% уропатогенных штаммов E.coli еще в начале 90-х были резистентны к ампициллину и цефалоспоринам I поколения [14]. В настоящее время этот уровень превышает 40% как в США, так и в европейских странах [7, 8]. Устойчивость E.coli, выделенной от пациентов с ИМП в России составляет от 31,6 до 51,5% в зависимости от популяции пациентов (Таблица 2).
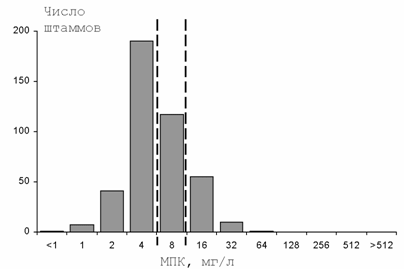
Несколько меньше данных накоплено по резистентности возбудителей ИМП к ингибиторзащищенным аминопенициллинам, в том числе к амоксициллину/клавуланату. В целом чувствительность уропатогенов к амоксициллину/клавуланату значительно выше, чем к ампициллину или амоксициллину. Однако, несмотря на относительной невысокий уровень резистентности (2,6-3,9%), в России выделяется достаточно много штаммов с промежуточной чувствительностью к этому антибиотику - 12,5-13% (Рисунок 2), в связи с этим, клиническая и микробиологическая эффективность этого антибиотика для терапии ИМП может быть недостаточно высокой. Большинство (>80%) энтерококков, выделенных от пациентов с ИМП в России чувствительны к ампициллину.
Рисунок 2. Распределение МПК амоксициллина/клавуланата для штаммов E.coli, выделенных от пациентов с неосложненными ИМП (пунктиром обозначены пограничные концентрации)
Сульфаметоксазол/триметоприм (ко-тримоксазол)
До 1990 гг резистентность к ко-тримоксазолу среди возбудителей внебольничных ИМП была низкой и не превышала 5% [11]. Однако в последние 10-15 лет отмечается четкая тенденцию к росту резистентности уропатогенной E coli к ко-тримоксазолу. Как было сказано выше, в США резистентность к этому антибиотику возросла за последние 20 лет с 7% до 18-20%. Аналогичная закономерность выявлена в Великобритании и Канаде [31, 13].
В России резистентность E coli, выделенной у пациентов с ИМП, к ко-тримоксазолу колеблется от 14,5% в случаях ИМП у беременных до 35,5% при ИМП у детей. У взрослых с неосложненными ИМП этот показатель составляет 21%. Очевидно, что уровень резистентности к этому антибиотику превысил критический уровень в 10-20%, что не позволяет рассматривать этот препарат в качестве терапии выбора при ИМП.
Одним из объяснений роста резистентности возбудителей ИМП к ко-тримоксазолу, является увеличение применения этого препарата для терапии и профилактики пневмоцистной пневмонии у ВИЧ инфицированных пациентов в последнее десятилетие [14] . Однако, в России, где также отмечается высокий уровень резистентности к этому антибиотику, его использование у ВИЧ инфицированных не получило такого распространения, как в США или Европе. На наш взгляд, объяснением высокого уровня резистентности уропатогенов к ко-тримоксазолу может быть неоправданно широкое применение этого антибиотика, особенно при респираторных инфекциях. Кроме того, ко-тримоксазол в России отпускается безрецептурно и часто применяется населением самостоятельно без каких-либо объективных показаний [15, 16].
Нефторированные (ранние, примитивные) хинолоны
В связи с разработкой более совершенных препаратов - фторхинолонов, интерес к нефторированным фторхинолонам, как препаратам для терапии ИМП, в настоящее время, незначительный. Нефторированные хинолоны уступают по микробиологической активности и фармакокинетическим характеристикам фторхинолонам. По данным исследований, выполненных в Европе, до 17% уропатогенной E.coli резистентны к налидиксовой кислоте [31]. В ряде городов Российской Федерации, например в Санкт-Петербурге, резистентность E.coli к хинолонам достигает 16-17%. Кроме того, для поддержания адекватных концентраций в моче ранние хинолоны необходимо принимать не реже 4 раз в сутки, что резко снижает комплаентность пациентов к этим уросептикам. Учитывая угрозу роста антибиотикорезистентности в целом и к возбудителям ИМП в частности, необходимо принимать во внимание свойство ранних хинолонов индуцировать развитие резистентности не только к самим ранним хинолонам, но и к фторхинолонам.
Фторхинолоны
Фторхинолоны, наряду с фосфомицином, являются препаратами, эффективность которых не уступает ко-тримоксазолу при терапии неосложненных ИМП короткими курсами. Фторхинолоны применяются в случае аллергии к ко-тримоксазолу или в тех регионах, где устойчивость к ко-тримоксазолу превышает 10-20%. Резистентность к фторхинолонам существенно различается в зависимости от региона. Так, в США на протяжении последних 10 лет отмечается низкий уровень устойчивости к фторхонолонам возбудителей ИМП и медленный рост резистености с 0,7% в 1995 до 2,5% в 2001 г. [14]. В некоторых странах Европы, таких как Испания, уровень резистентности к фторхинолонам возбудителей внебольничных ИМП может достигать 15% (Таблица 1). В России уровень резистености к фторхинолонам (ципрофлоксацину, норфлоксацину) относительно низкий - 4,3% (Таблица 2).
Фторхинолоны сохраняют высокую активность в отношении других грам(-) возбудителей ИМП. Отмечается относительно высокая резистентность энтерококков к фторхинолонам (20-40%), однако этиологическая роль этих возбудителей для амбулаторных ИМП невелика. S saprophyticus, как правило, чувствителен к большинству фторхинолонов, МПК ципрофлоксацина и офлоксацина несколько выше, чем других препаратов этой группы [26].
Нитрофурантоин
Нитрофурантоин - один из самых старых антимикробных препаратов, и, тем не менее, уровень резистентности к этому антибиотику остается невысоким в течении нескольких десятилетий. В странах Европы и США устойчивость уропатогенной E.coli к нитрофурантоину не превышает 1-2% [7]. По нашим данным, в России резистентность к этому антибиотику составляет 1,2-4,3% в зависимости от популяции пациентов (Таблица 2).
Такое медленное развитие резистености объясняется несколькими факторами. С одной стороны, у нитрофурантоина существует несколько механизмов действия, поэтому, для развития резистентности, у бактерии должны одновременно развиться несколько мутаций. С другой стороны, нитрофурантоин имеет ограниченное применение при ИМП в силу относительно плохой переносимости и безопасности, а также фармакокинетических особенностей - нитрофурантоин не накапливается в высоких концентрациях в паренхиме почек. Поэтому этот антибиотик показан только при остром неосложненном цистите.
Уровень резистентности других грам(-) уропатогенов, например K. pneumoniae, к нитрофурантоину выше, чем у E. coli [7]. Нитрофурантоин остается активным и в отношении грам(+) возбудителей ИМП, например S. saprophyticus и энтерококков, включая ванкомицинрезистентные штаммы.
Нитроксолин
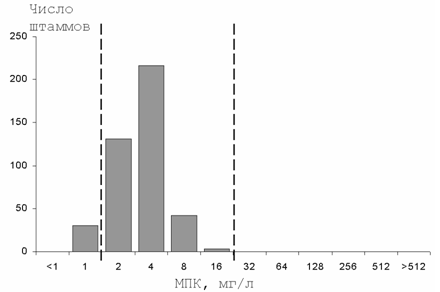
Нитроксолин - устаревший антисептик, которые более 20 лет снят с производства в большинстве стран мира. Соответственно, исследования по изучению резистентности уропатогенов к этому препарату не проводятся. Критерии интерпретации чувствительности микроорганизмов к нитроксолину не пересматриваются уже более 15 лет. Учитывая, что этот препарат все еще применяется в России и странах СНГ, нами проводилось изучение чувствительности уропатогенов к нитроксолину в ходе проектов UTIAP-1 и UTIAP-2. Полученные данные позволяют утверждать, что 92,9% штаммов E.coli нечувствительны к данному антибиотику. Как видно из гистограммы распределения МКП (Рисунок 3), даже при неосложненных ИМП практически вся популяция E.coli находится в зоне промежуточной резистентности к нитроксолину, что свидетельствует о низкой микробиологической активности препарата и несовершенстве критериев интерпретации чувствительности.
Рисунок 3. Распределение МПК нитроксолина для штаммов E.coli, выделенных от пациентов с неосложненными ИМП (пунктиром обозначены пограничные концентрации), Россия, 2000-01 гг.
Фосфомицин
Фосфомицина трометамол - один из новых антимикробных препаратов, разработанных для терапии ИМП, в первую очередь - острого неосложненного цистита. Фосфомицин - единственный препарат, который обладает достаточно высокой эффективность при терапии острого цистита одной дозой. Фосфомицин является антибиотиком широкого спектра действия, активным в отношении большинства аэробных грам(-) и грам(+) бактерий. В исследованиях in vitro показано, что при концентрации, достигаемой фосфомицином в моче, большинство возбудителей ИМП, включая ванкомицин-резистентных энтерококков, чувствительны к этому антибиотику.
В Европе, несмотря на широкое применение препарата, резистентность к нему очень низкая и колеблется от 0 до 1,5% [8]. Подобно нитрофурантоину, фосфомицин сохраняет свою активность и в случае инфекций, вызванных возбудителями, резистентными к другим антибиотикам. Было показано, что 100% фторхинолон-резистентных уропатогенных E. coli чувствительны к фосфомицину [27]. Вероятно, такая особенность фосфомицина объясняется наличием нескольких механизмов действия. Благодаря уникальному механизму действия фосфомицина, практически не встречается перекрестная резистентность с другими антибиотиками.
По данным многоцентровых российских исследований (UTIAP, ARMID, ARIMB), не выявлено штаммов E.coli, резистентных к фосфомицину (Таблица 2). Данные полученные в России вполне согласуются с данными, полученными в крупных зарубежных многоцентровых микробиологических исследованиях, таких, как ECO-SENS [8], свидетельствующие о крайне низкой (0-1%) частоте выделения устойчивых к фосфомицину штаммов.
Влияние антибиотикорезистентности на эффективность терапии ИМП
Способность микроорганизмов формировать устойчивость к антибиотикам сопряжена с рядом негативных последствий, как для отдельных пациентов, так и для общества в целом. При устойчивости возбудителя инфекции к антибиотикам резко возрастает вероятность неудачи эмпирического лечения конкретного пациента. Назначить адекватную терапию и предотвратить неблагоприятный исход возможно при своевременном получении данных о спектре и уровне антибиотикорезистентности возбудителя. В то же время, каждое конкретное заболевание, вызываемое резистентным микроорганизмом, является проявлением процесса формирования и распространения устойчивости в микробной популяции.
До настоящего времени существовал некоторые сомнения относительно влияния резистентности уропатогенов, выявляемой in vitro на клиническую и микробиологическую эффективность антибиотикотерапии ИМП, так как известно, что уроантисептики, создают достаточно высокие концентрации в моче. В последние годы получены данные, доказывающие снижение клинической эффективности антибиотика, в частности ко-тримоксазола, в случае широкого распространения резистентных штаммов.
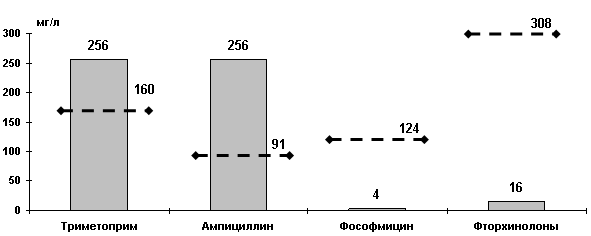
Оказалось, что МПК для большинства штаммов E coli, резистентных к ко-тримоксазолу выше, чем концентрации этого антибиотика в моче [17]. Исследования по изучению чувствительности возбудителей ИМП в России позволили рассчитать МПК[1] и МПК90 основных антибиотиков, применяемых для терапии ИМП и сравнить их с пиковыми концентрациями в моче (Рисунок 4). Пиковые концентрации триметоприма (основного и наиболее активного компонента ко-тримоксазола) и ампициллина в моче ниже МПК90 штаммов E.coli, выделенных у пациентов с ИМП. Напротив, фосфомицин и фторхинолоны накапливаются в моче в очень высоких концентрациях, позволяющих превысить МПК90 в 31 и 19 раз, соответственно. Таким образом, ко-тримоксазол и ампициллин в большинстве случаев не создают в моче концентраций достаточных для эрадикации возбудителя.
Рисунок 4. МПК90 (по данным исследования UTIAP-2, Россия, 2000-01 гг) и пиковые концентрации антибиотиков в моче [17, 20, 21, 22]. Значения МПК90 представлены столбиками, соответствующие пиковые концентрации антибиотиков - пунктирными линиями.
Наибольший интерес и убедительность имеют данные, полученные в больших проспективных исследованиях, спланированных специально для того, чтобы выяснить влияние антибиотикорезистености на клиническую эффективность терапии ИМП. В одном из исследований, проведенном в Израиле, где профиль антибиотикорезистентности во много сходен с Россией, анализировали клиническую и микробиологическую эффективность терапии ко-тримоксазолом 960 мг дважды в день у женщин с острым неосложненным циститом (ОНЦ) в зависимости от наличия или отсутствия у возбудителя устойчивости к ко-тримоксазолу [23]. Всем пациенткам до начала терапии проводили микробиологическое исследование мочи, а выделенные возбудители тестировали на чувствительность к антибиотикам, в том числе и ко-тримоксазолу. Оказалось, что клиническая эффективность терапии (улучшение) составила 88% в случае ОНЦ, вызванного чувствительными штаммами, и 54%, если заболевание вызывали резистентные бактерии, различия были статистически достоверными (Рисунок 5). При анализе бактериологической эффективности были выявлены еще большие различия - эрадикация возбудителя достигалась в 86% случаев, если уропатогены были чувствительны и только в 42%, если резистентны.
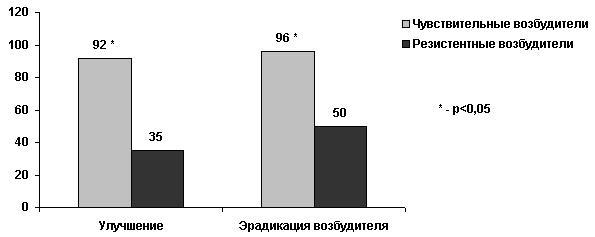
Аналогичные данные были получены при изучении пациентов с острым пиелонефритом (Рисунок 6) [24]. В многоцентровом рандомизированном исследовании, выполненном в США, женщины с острым внебольничным пиелонефритом получали терапию либо ципрофлоксацином 500 мг 2 раза в день в течение 7 дней, либо ко-тримоксазолом 960 мг 2 раза в день в течение 14 дней. При оценке бактериологической эффективности, оказалось, что если инфекция была вызвана чувствительным к ко-тримоксазолу штаммом, то частота эрадикации составляла 96%, а если резистентным, то 50% (p<0,05). Кроме того, было установлено, что в случае пиелонефрита, вызванного резистентным уропатогеном, клиническая эффективность снижается с 92% до 35% (p<0,05).
Рисунок 5. Клиническая (улучшение) и микробиологическая (эрадикация возбудителя) эффективность терапии ОНЦ ко-тримоксазолом в зависимости от наличия или отсутствия резистентности у возбудителей [23]
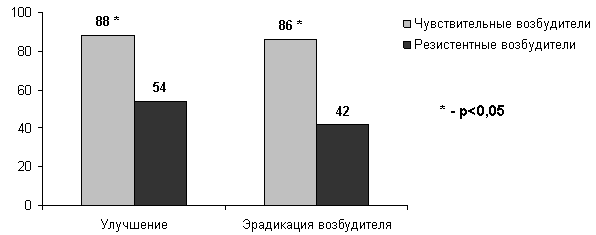
Рисунок 6. Клиническая (улучшение) и микробиологическая (эрадикация возбудителя) эффективность терапии пиелонефрита ко-тримоксазолом в зависимости от наличия или отсутствия резистентности у возбудителей [24]
Таким образом, в настоящее время накоплены убедительные данные, полученные как в исследованиях in vitro, так и в клинических испытаниях, позволяющие утверждать, что клиническая, и микробиологическая эффективность антибиотиков в 1,6-3 раза ниже у пациентов с ИМП, вызванными резистентными возбудителями.
Факторы риска антибиотикорезистентности возбудителей ИМП
Учитывая, что в случае ИМП, вызванных резистентными штаммами эффективность терапии может существенно снижаться, для врача важно иметь представление о факторах, прогнозирующих случаи инфекции, вызванной резистентными к тем или иным антибиотикам уропатогенами.
Наиболее детально изучены факторы риска развития ИМП, вызванных уропатогенами, резистентными к ко-тримоксазолу. В нескольких исследованиях [9, 10], выполненных по типу случай-контроль, были проанализированы предполагаемые факторы риска выделения резистентного возбудителя ИМП (Таблица 3).
Таблица 3. Факторы риска развития ИМП, вызванных резистентными к ко-тримоксазолу уропатогенами [9, 10]
Фактор риска Отношение шансов Прием ко-тримоксазола в течение 3-6 месяцев предшествующих эпизоду ИМП 5,1 Прием любых антибиотиоков в течение 3 месяцев предшествующих эпизоду ИМП 4,5 Сахарный диабет 3,1 Госпитализация, предшествующая эпизоду ИМП 2,5 Оказалось, что шанс развития ИМП, вызванных резистентными к ко-тримоксазолу возбудителями, был в 5,1 раз выше у женщин, получавших ко-тримоксазол по поводу текущего эпизода ИМП или в течение 3 месяцев до этого эпизода. Соответственно, шанс развития ИМП, вызванных резистентными к ко-тримоксазолу возбудителями в 4,5 раза выше у пациентов, которым в течение 3 предшествующих месяцев назначали любые антибиотики, в 3,1 раза выше при наличии диабета, и в 2,5 раза выше при наличии в анамнезе госпитализаций. Возраст, предшествующие эпизоды ИМП, онкологические заболевания, хроническая неврологическая патология не были достоверно связаны с повышением риска антибиотикорезистентности к ко-тримоксазолу.
При более детальном анализе оказалось, что при исключении влияния предшествующих госпитализаций, диабет не является независимым фактором риска антибиотикорезистентности. Предполагается, что более частое выделение резистентных уропатогенов у пациентов страдающих диабетом может быть связано с более высокой частотой госпитализаций.
Заключение
Таким образом, основным возбудителем амбулаторных ИМП является E.coli. Рост резистентности этого возбудителя обуславливает снижение эффективности антибиотикотерапии, поэтому данные по изучению устойчивости E.coli к антибиотикам лежат в основе современной концепции выбора препаратов для терапии ИМП. В России, как и в большинстве стран мира, отмечается рост резистентности E.coli к аминопенициллинам и ко-тримоксазолу, что заставляет пересматривать место этих антибиотиков в терапии амбулаторных ИМП. В качестве препаратов выбора необходимо рассматривать, в первую очередь, антибиотики с высокой микробиологической активностью - фосфомицин и фторхинолоны.
Литература
- Gupta K. Addressing Antibiotic Resistance Am J Med 2002; 113 (1A): 29S-34S
- Warren J.W., Abrutyn E., Hebel J.R., e.a. Guidelines for antimicrobial treatment of uncomplicated acute bacterial cystitis and acute pyelonephritis in women. Infectious Diseases Society of America (IDSA). Clin. Infect. Dis 1999; 29: 745-58.
- Gupta K, Scholes D, Stamm WE. Increasing prevalence of antimicrobial resistance among uropathogens causing acute uncomplicated cystitis in women. JAMA. 1999;281: 736-738.
- Gupta K, Sahm DF, Mayfield D, Stamm WE. Antimicrobial resistance among uropathogens that cause community acquired urinary tract infections in women: a nationwide analysis. Clin Infect Dis. 2001;33:89-94.
- Dyer IE, Sankary TM, Dawson JA. Antibiotic resistance in bacterial urinary tract infections, 1991 to 1997. West J Med. 1998;169:265-268.
- Naber K.G., Bergman B., Bishop M.C., et al., for the Urinary Tract Infection (UTI) Working Group of the Health Care Office (HCO) of the European Association of Urology (EAU). EAU guidelines for the management of urinary and male genital tract infections. Eur Urol 2001; 40: 576-588.
- Gupta K. Emerging antibiotic resistance in urinary tract pathogens. Infect Dis Clin North Am. 2003; 17(2) :243-59.
- Kahlmeter G. An International Survey of the Antimicrobial Susceptibility of pathogens from Uncomplicated Urinary Tract Infections: the ECO-SENS Project. J Antimicrob. Chemother., 2003; 51 (1): 69-76.
- Wright S.W., Wrenn K.D., Haynes M.L. Trimethoprim-sulfamethoxazole resistance among urinary coliform isolates. J Gen Intern Med. 1999; 14: 606-609.
- Steinke D.T., Seaton R.A., Phillips G., MacDonald T.M., Davey P.G. Factors associated with trimethoprim-resistant bacteria isolated from urine samples. J Antimicrob Chemother. 1999; 43: 841-843.
- Hooton T.M., Latham R.H., Wong E.S., Johnson C., Roberts P.L., Stamm W.E. Ofloxacin versus trimethoprim-sulfamethoxazole for treatment of acute cystitis. Antimicrob Agents Chemother 1989; 33(8): 1308-12.
- Winstanleya T.G., Limba D.I., Eggingtona R., Hancockb F. A 10 year survey of the antimicrobial susceptibility of urinary tract isolates in the UK: the Microbe Base project. J Antimicrob Chemother 1997; 40: 591-594.
- Zhanel G.G., Karlowsky J.A., Harding G.K., Carrie A., Mazzulli T., Low D.E., et al. A Canadian national surveillance study of urinary tract isolates from outpatients: comparison of the activities of trimethoprim- sulfamethoxazole, ampicillin, mecillinam, nitrofurantoin, and ciprofloxacin. The Canadian Urinary Isolate Study Group. Antimicrob Agents Chemother 2000; 44(4):1089-92.
- Karlowsky J.A., Kelly L.J., Thornsberry C., Jones M.E., Sahm D.F. Trends in antimicrobial resistance among urinary tract infection isolates of Escherichia coli from female outpatients in the United States. Antimicrob Agents Chemother 2002; 46(8): 2540-5.
- Козлов С.Н., Рачина С.А., Домникова Н.П., Карпов О.И., Кузин В.Б., Лещенко И.В. и др. Фармакоэпидемиологический анализ лечения внебольничной пневмонии в амбулаторных условиях. Клиническая микробиология и антимикробная химиотерапия, 2000; №3: 74-81.
- Андреева И.В., Рачина С.А., Петроченкова Н.А., Галкин Д.В., Горенкова Е.В. и др. Самостоятельное применение антимикробных препаратов населением: результаты многоцентрового исследования. Клиническая фармакология и терапия, 2002; №3: 15-26.
- Davidson R., Fuller J., Mazzulli T., Porter-Pong S., McGeer A., Low D.E. High-level trimethoprim-sulfamethoxazole resistance in community-acquired urinary tract gram-negative isolates. Presented at the 38th Interscience Conference on Antimicrobial Agents and Chemotherapy. San Diego, CA, September 24-27, 1998.
- McCarty J.M., Richard G., Huck W., Tucker R.M., Tosiello R.L., Shan M., et al. A randomized trial of short-course ciprofloxacin, ofloxacin, or trimethoprim/sulfamethoxazole for the treatment of acute urinary tract infection in women. Ciprofloxacin Urinary Tract Infection Group. Am J Med 1999; 106(3): 292-9.
- Brown P.D., Freeman A., Foxman B.. Prevalence and predictors of trimethoprim-sulfamethoxazole resistance among uropathogenic Escherichia coli isolates in Michigan. Clin Infect Dis 2002; 34(8): 1061-6.
- Shrestha N. K., Tomford J. W. Fosfomycin: a review. Infect Dis Clin Pract 2001;10:255-260.
- Henry D.C., Bettis R.B., Riffer E., Haverstock D.C., Kowalsky S.F., Manning K., Hamed K.A., Church D.A.. Comparison of once-daily extended-release ciprofloxacin and conventional twice-daily ciprofloxacin for the treatment of uncomplicated urinary tract infection in women.. Clin Ther 2002;24(12):2088-104.
- Meyers B.R., Wilkinson P., Mendelson M.H., Walsh S., Bournazos C., Hirschman S.Z. Pharmacokinetics of ampicillin-sulbactam in healthy elderly and young volunteers. Antimicrob Agents Chemother. 1991; 35(10): 2098-101.
- Raz R., Chazan B., Kennes Y., Colodner R., Rottensterich E., Dan M., et al. Empiric use of trimethoprim-sulfamethoxazole (TMP-SMX) in the treatment of women with uncomplicated urinary tract infections, in a geographical area with a high prevalence of TMP-SMX-resistant uropathogens. Clin Infect Dis 2002; 34(9): 1165-9.
- Talan D.A. Stamm W.E., Hooton T.M., Moran G.J., Burke T., Iravani A., et al.Comparison of ciprofloxacin (7 days) and trimethoprim-sulfamethoxazole (14 days) for acute uncomplicated pyelonephritis pyelonephritis in women: a randomized trial. JAMA 2000; 283(12): 1583-90.
- Rafalski V., Ahmetova L., Babkin P., Kogan M. e.a. Antibiotic drug prescription in community-acquired urinary tract infection: a Russian multicenter pharmacoepidemiological survey // 23 Intrenational Congress of Chemotherapy, Durban, South Africa, 7-9 June 2003.- Abs. SA 113.- P. 4.
- Hoban D.J., Bouchillon S.K., Johnson J.L., Zhanel G.G., Butler D.L., Miller L.A., et al. Comparative in vitro activity of gemifloxacin, ciprofloxacin, levofloxacin and ofloxacin in a North American surveillance study. Diagn Microbiol Infect Dis 2001;40(1-2):51-7.
- Ungheri D., Albini E., Belluco G. In-vitro susceptibility of quinolone-resistant clinical isolates of Escherichia coli to fosfomycin trometamol. J Chemother 2002; 14(3): 237-40.
- Nicolle L.E. Epidemiology of Urinary Tract Infection. Infect Med, 2001; 18: 153-162.
- Nicolle L. A Practical Guide to Antimicrobial Management of Complicated Urinary Tract Infection. Drugs Aging, 2001; 18: 243-254.
- Рафальский В.В., Страчунский Л.С., Кречикова О.И., Эйдельштейн И.А., Ахметова Л.И., Бабкин П.А. и др. Резистентность возбудителей амбулаторных инфекций мочевыводящих путей по данным многоцентровых микробиологических исследований UTIAP-I и UTIAP-II. Урология 2004; 2: 10-16.
- Winstanleya T.G., Limba D.I., Eggingtona R., Hancockb F. A 10 year survey of the antimicrobial susceptibility of urinary tract isolates in the UK: the Microbe Base project. J Antimicrob Chemother 1997; 40: 591-4.
| Август 2009 г. |