Опубликовано в:
«СПРАВОЧНИК ПОЛИКЛИНИЧЕСКОГО ВРАЧА» »» 2013 № 4
Нимесулид: мифы и реальность
А.Е.Каратеев
ФГБУ НИИ ревматологии РАМН, Москва
В настоящий момент врачи располагают богатым арсеналом средств борьбы с острой и хронической болью. Проблема иногда заключается в том, что и какому пациенту предложить. По мнению многих экспертов, нестероидные противовоспалительные препараты (НПВП) должны рассматриваться как средство 1-й линии, к которому следует обратиться во всех клинических ситуациях, когда боль носит ноцицептивный характер, т.е. связана с воспалением или повреждением живой ткани. Применение анальгетических средств с иным механизмом действия, таких как опиоиды, миорелаксанты, средства для лечения нейропатической боли и другие, оправданно лишь в той ситуации, когда НПВП оказались малоэффективными или имеются серьезные противопоказания для их назначения.
Ключевым механизмом воздействия НПВП на периферическую и центральную составляющую хронической боли является блокада фермента циклооксигеназы (ЦОГ)-2 и подавление гиперпродукции простагландинов (ПГ). НПВП являются основным средством для лечения боли у пациентов с ревматическими заболеваниями (РЗ): остеоартрозом (ОА), болью в нижней части спины, ревматоидным артритом (РА), анкилозирующим спондилитом. Конечно, современная терапия заболеваний суставов и позвоночника не основывается лишь на применении обезболивающих препаратов. Напротив, главное направление современного противоревматического лечения - остановка прогрессирования заболевания, подавление хронического воспаления и прекращение разрушения суставов. И эта задача благодаря революционным достижениям современной науки и внедрению в ревматологическую практику новых чрезвычайно эффективных патогенетических средств (таких как генно-инженерные биологические препараты), сегодня может быть решена. Тем не менее обезболивающие препараты продолжают сохранять свое место в комплексной терапии патологии суставов и позвоночника - в качестве вспомогательного, но незаменимого средства.
Необходимость проведения активной анальгетической терапии при РЗ определяется тем фактом, что хроническая боль независимо от этиологии становится самостоятельной угрозой для жизни пациента. Типичными спутниками хронической боли становятся депрессия, тревожность, нарушения сна и иммунитета, постоянное напряжение сердечно-сосудистой системы (ССС). Поэтому представления о том, что боль надо перетерпеть или научиться жить с ней, сегодня считают вредными и порочными.
Применение НПВП и качество жизни больных с РЗ
С точки зрения пациентов, НПВП являются важнейшим средством, позволяющим контролировать их состояние. В этом плане весьма любопытной представляется работа австралийских ученых, оценивших мнение пожилых людей, страдающих ОА, о разных анальгетиках. Само название статьи It looks after me (они заботятся обо мне) показывает позитивный настрой пациентов в отношении этих лекарств. По мнению больных, НПВП весьма эффективны - они хорошо устраняют симптомы болезни, позволяя сохранять повседневную активность. При этом в отличие от популярного безрецептурного анальгетика парацетамола они гораздо удобнее (нет необходимости принимать ежедневно несколько таблеток). В сравнении с опиоидами (они малодоступны у нас, но широко используются для купирования боли при РЗ на Западе) НПВП гораздо лучше переносятся, что имеет принципиальное значение для пожилых людей.
Очень важно, что активное применение НПВП способно не только улучшить качество жизни, но и повысить выживаемость пациентов с хроническими РЗ. В качестве доказательства данного положения можно привести работу T.Lee и соавт. Эти ученые наблюдали когорту 565 454 ветеранов США, страдающих ОА. Оказалось, что больные, регулярно принимавшие НПВП, достоверно реже (более 20%) погибали от кардиоваскулярных катастроф в сравнении с теми, кто не принимал этих препаратов.
Побочные действия НПВП
Однако применение НПВП - палка о двух концах, ведь эти препараты способны вызывать серьезные, угрожающие жизни осложнения, что может существенно ограничивать их терапевтическую ценность.
Желудочно-кишечный тракт
Традиционно на первое место среди этих осложнений ставят НПВП-гастропатию - специфическую патологию верхних отделов желудочно-кишечного тракта (ЖКТ), характеризующуюся появлением эрозий слизистой оболочки, язв и гастроинтестинальных катастроф - кровотечения и перфорации. Согласно общепризнанной теории этот побочный эффект возникает вследствие неселективности НПВП в отношении ЦОГ: помимо «плохой» (индуцируемой) ЦОГ-2 они блокируют также «хорошую» (структурную, постоянно присутствующую в тканях) ЦОГ-1, снижая тем самым синтез цитопротективных ПГ слизистой оболочки ЖКТ и способствуя ее повреждению под действием кислоты желудочного сока. Риск развития такой патологии у лиц, регулярно принимающих неселективные ингибиторы ЦОГ-2 (н-НПВП), возрастает по сравнению с популяцией более чем в 4 раза и составляет примерно 0,5-1 эпизод на 100 пациентов в год. По представлениям 1990-х годов больные, регулярно получавшие НПВП, погибали от ЖКТ-кровотечений в 2-3 раза чаще в сравнении с людьми, не принимающими каких-либо препаратов этой лекарственной группы.
РЕЖИМ ДОЗИРОВАНИЯ НАЙЗ®
Таблетки принимают с достаточным количеством воды предпочтительно после еды.
Взрослым и детям старше 12 лет - внутрь по 1 таблетке 2 раза в сутки. При наличии заболеваний желудочно-кишечного тракта препарат желательно принимать в конце еды или после приема пищи.
Максимальная суточная доза для взрослых - 200 мг.
Пациентам с хронической почечной недостаточностью требуется снижение суточной дозы до 100 мг
Представлена краткая информация производителя по дозированию лекарственного средства.
Перед назначением препарата внимательно читайте инструкцию.
Сердечно-сосудистая система
В последние годы принципиальное значение в оценке безопасности НПВП придается риску развития опасных осложнений со стороны ССС - инфаркта миокарда, внезапной коронарной смерти и ишемического инсульта (кардиоваскулярные катастрофы). Опасность тяжелых осложнений со стороны ССС существенно увеличивается у пациентов, в течение длительного времени и регулярно принимающих высокие дозы НПВП. Эта патология возникает вследствие влияния НПВП на баланс синтеза тромбоксана А2 (ЦОГ-1-зависимый процесс) и простациклина (ЦОГ-2-зависимый процесс) - субстанций, обладающих про- и антитромботическим действием.
Ранее считалось, что развитие этой патологии характерно в большей степени для селективных ингибиторов ЦОГ-2 (с-НПВП). Но теперь уже не вызывает сомнений тот факт, что и применение многих н-НПВП (в частности, диклофенака и индометацина) также способно повышать риск опасных осложнений со стороны ССС.
Кроме прокоагулянтного действия, НПВП способны вызывать дестабилизацию артериальной гипертензии (АГ), и это важный момент в патогенезе кардиоваскулярных катастроф. Данное осложнение в большей степени связано с блокадой ЦОГ-2 (а не ЦОГ-1, как думали ранее), которая образуется клетками почек в условиях повышенного артериального давления (АД). В этой ситуации ПГ, синтезируемые благодаря активности ЦОГ-2, играют роль важного фактора контроля АГ.
Факторы риска НПВП-осложнений
Подавляющее большинство серьезных побочных эффектов, связанных с приемом НПВП (как со стороны ЖКТ, так и ССС), возникают у больных, имеющих так называемые факторы риска (рис. 1).
Рис. 1. Факторы риска НПВП-осложнений.
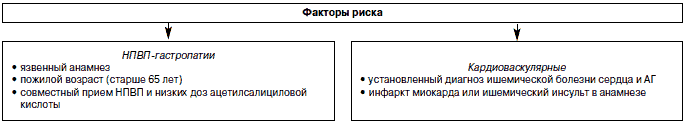
К сожалению, эти факторы очень часто присутствуют у пожилых больных, которые составляют основную часть современной популяции, нуждающейся в активной обезболивающей терапии.
Группа НПВП
Спектр НПВП, представленных сегодня на российском фармакологическом рынке, весьма широк - он насчитывает 18 разных наименований: ацетилсалициловая кислота, ацеклофенак, декскетопрофен, диклофенак, ибупрофен, кетопрофен, кеторолак, лорноксикам, мелоксикам, метамизол, напроксен, нимесулид, пироксикам, теноксикам, фенилбутазон, флубипрофен, целекоксиб и эторикоксиб.
Такое обилие препаратов делает возможным подбор конкретного средства для любой клинической ситуации и каждого конкретного специалиста. Главными факторами, которые учитываются практикующими врачами, является наличие у лекарства быстрого и мощного обезболивающего эффекта, противовоспалительного действия и хорошей переносимости. При этом очень важно, чтобы этот препарат имел достаточно низкий риск развития осложнений -как со стороны ЖКТ, так и ССС. Ведь по меткому замечанию академика Е.Л.Насонова, подбор обезболивающего препарата при РЗ - «путешествие между Сциллой и Харибдой».
Нимесулид
Принципиально важно, чтобы препарат имел невысокую стоимость, делающую его доступным широкому кругу потребителей.
Сочетание этих параметров свойственно нимесулиду -весьма популярному в России представителю группы НПВП. Важным критерием предпочтения практикующих врачей является уровень продаж препарата. Так, с 2006 по 2010 г. продажи нимесулида поднялись с 7 до 18 млн упаковок в год; в этом плане он уступает лишь диклофенаку с его обилием дешевых генериков (около 100 наименований!) и безрецептурному ибупрофену.
Высокий интерес к нимесулиду среди практикующих врачей сохраняется и в ряде стран Восточной и Центральной Европы. По данным A.Inotai и соавт., за период с 2002 по 2007 г., использование двух самых применяемых препаратов из группы с-НПВП - нимесулида и мелоксикама -выросло в этих странах на 325%.
Нимесулид - эффективное и удобное средство для лечения острой боли. У него высокая биодоступность - через 30 мин после перорального приема достигается значимая концентрация препарата в крови (не менее 25% от максимальной). Соответственно, уже через 30 мин препарат начинает работать, а через 1-3 ч развивается полный обезболивающий эффект.
Как было отмечено, фармакологическое действие НПВП связано с подавлением активности ЦОГ-2, а ассоциированные с их приемом осложнения со стороны ЖКТ в основном определяются блокадой ЦОГ-1 в слизистой ЖКТ. Однако ЦОГ-1 также принимает участие в развитии воспаления, поэтому локальное снижение ее активности в области повреждения следует рассматривать как позитивный момент. Нимесулид, обладающий умеренной селективностью в отношении ЦОГ-2, имеет подобное действие: лишь в небольшой степени влияя на «структурную» ЦОГ-1 слизистой желудка, он существенно снижает ее эффекты в области воспаления.
По мнению экспертов, есть основание предполагать для нимесулида ряд фармакологических эффектов, не зависимых от класс-специфического воздействия на ЦОГ-2. Так, он снижает гиперпродукцию основных провоспалительных цитокинов (интерлейкин-6, фактор некроза опухоли a), подавляет активность металлопротеиназ (ответственных, в частности, за разрушение гликопротеинового комплекса хрящевой ткани при ОА), обладает антигистаминным действием. Одним из важнейших «не-ЦОГ2-ассоциированных эффектов» нимесулида является блокада фермента фосфодиэстеразы-4, подавляющая активность макрофагов и нейтрофилов, которые играют важную роль в патогенезе острой воспалительной реакции.
Доказательная база
Терапевтический потенциал нимесулида доказан в ходе многочисленных клинических исследований. Так, имеются данные по его использованию при послеоперационном обезболивании. Например, в исследовании A.Binning и соавт. 94 пациентам, перенесшим артроскопическую операцию, в качестве анальгетика на 3 дня назначались нимесулид 200 мг, напроксен 1000 мг или плацебо. Согласно результатам исследования оба НПВП демонстрировали превосходство над плацебо. Но нимесулид в сравнении с препаратом контроля обеспечивал более высокий обезболивающий эффект в первые 6 ч после операции.
При острой патологии околосуставных мягких тканей - энтезитах, бурситах и тендинитах - нимесулид показал столь же выраженный (или даже несколько более высокий) эффект в отношении купирования боли и восстановления функции опорно-двигательной системы по сравнению с высокими дозами «традиционных» НПВП - диклофенака и напроксена. Например, в исследовании W.Wober 122 пациента с субакромиальным бурситом и тендинитом в течение 14 дней принимали нимесулид 200 мг/сут или диклофенак 150 мг/сут. В конце периода наблюдения хороший или отличный эффект терапии несколько чаще отмечался у получавших нимесулид - 82,3% в сравнении с 78,0% применяющих диклофенак. Субъективная оценка пациентов в отношении переносимости лекарств демонстрировала еще более значимое преимущество нимесулида. При этом 96,8% больных оценили переносимость нимесулида как хорошую или отличную и лишь 72,9% дали аналогичную оценку диклофенаку (p<0,05).
Нимесулид оказался действенным средством для лечения неспецифической боли в нижней части спины. Согласно результатам исследования, проведенного в Финляндии (n=102), нимесулид 100 мг 2 раза в сутки превосходил ибупрофен в дозе 600 мг 3 раза в сутки как по выраженности обезболивающего эффекта, так и по восстановлению функции позвоночника. К 10-му дню от начала лечения на фоне приема нимесулида отмечалось более чем двукратное улучшение функциональной активности. Среди пациентов, принимавших этот препарат, индекс Остверсти в среднем снизился с 38 до 15 баллов (-23), что достоверно отличалось от ибупрофена - с 35 до 20 (-15), р=0,02. При этом в сравнении с препаратом контроля нимесулид существенно реже (примерно в 2 раза - 7 и 13% соответственно) вызывал побочные эффекты со стороны ЖКТ.
Последнее крупное и хорошо организованное исследование, в котором оценивалась эффективность нимесулида, было проведено сербскими учеными L.Konstantinovic и соавт. Вообще эта работа посвящена применению низкоэнергетической лазерной терапии при острой боли в спине, сопровождающейся компрессией седалищного нерва (люмбоишалгия). Однако авторы оценивали эффективность лазеротерапии у больных, которые одновременно принимали НПВП - нимесулид в дозе 200 мг/сут. Всего в исследование были включены 546 больных, которые составили 3 группы: в 1-й пациенты получали нимесулид + настоящую лазеротерапию, 2-й - только нимесулид, 3-й - сочетание этого препарата и ложной лазеротерапии (плацебо). Согласно данным исследования в 1-й группе эффект был максимальным - уровень обезболивания достоверно превосходил результаты, полученные в 2 контрольных группах. Тем не менее весьма интересно отметить тот факт, что нимесулид сам по себе (2-я группа) и в комбинации с плацебо лазера давал весьма существенное облегчение не только механической боли в спине, но и радикулярной (нейропатической). Так, боль в спине уменьшилась в среднем в каждой из групп на 44, 18 и 22 мм, а в ноге - 33, 17 и 20 мм (визуальная аналоговая шкала). При этом переносимость терапии оказалась весьма хорошей - авторы не сообщили ни об одном случае серьезных осложнений, связанных как с использованием лазера, так и нимесулида.
Помимо острой боли нимесулид зарекомендовал себя как эффективное симптоматическое средство при хронических РЗ, прежде всего ОА. Так, P.Locker и соавт. провели сравнение нимесулида 200 мг или этодолака 600 мг у 199 больных ОА в ходе 3-месячного исследования. Лечебное действие нимесулида оказалось более высоким - его оценили как хорошее или превосходное 80% больных и лишь 68% дали аналогичную оценку этодолаку.
В масштабном и более длительном (6 мес) исследовании E.Huskisson и соавт. нимесулид в дозе 200 мг/сут сравнивали с диклофенаком 150 мг/сут у 279 больных ОА. Лечебное действие исследуемых препаратов, которое оценивалось по динамике самочувствия больных и функциональному индексу Лекена, практически не различалось. Однако переносимость нимесулида была достоверно лучше - в частности, осложнения со стороны ЖКТ возникли у 36 и 47% больных соответственно (p<0,05).
Самым крупным из длительных исследований нимесулида стала работа W.Kriegel и соавт., которые оценивали эффективность и безопасность этого препарата в сравнении с напроксеном 750 мг у 370 больных ОА в течение 1 года. Аналогично результатам, полученным E.Huskisson, эффективность обоих препаратов оказалась сопоставимой, правда, с некоторым преимуществом нимесулида. Так, изменение суммарного индекса WOMAC ко времени завершения работы составило 22,5 и 19,9%. Суммарная частота побочных эффектов при использовании нимесулида в сравнении с напроксеном также оказалась ниже - 47,5 и 54,5% соответственно. Следует обратить внимания на тот факт, что во всех трех исследованиях на фоне приема нимесулида не было зафиксировано значимого увеличения кардиоваскулярных осложнений.
Переносимость и безопасность
Однако важнейшим достоинством нимесулида является хорошая переносимость и относительно низкая частота развития осложнений со стороны ЖКТ. Хорошо известно, что именно развитие патологии ЖКТ, относящейся к числу класс-специфических осложнений НПВП, является одним из основных факторов, определяющих соотношение риск/польза для этого класса лекарственных препаратов. Данные, подтверждающие благоприятную переносимость нимесулида в отношении ЖКТ, были получены российскими и зарубежными учеными в ходе серии проспективных и когортных наблюдательных исследований.
Очень показательна работа ирландского ученого F.Bradbury, который провел оценку частоты ЖКТ-осложнений при использовании диклофенака (n=3553), нимесулида (n=3807) и ибупрофена (n=1470) в реальной клинической практике. Суммарная частота этой патологии при использовании нимесулида была существенно меньше в сравнении с диклофенаком - 12,1%, хотя и не отличалась от ибупрофена - 8,1 и 8,6%.
Относительно низкий риск развития ЖКТ-осложнений при использовании нимесулида также был подтвержден работой итальянских эпидемиологов A.Conforti и соавт., которые провели анализ 10 608 спонтанных сообщений о серьезных побочных эффектах (1988-2000 гг.), связанных с приемом разных НПВП. Нимесулид, как оказалось, был причиной развития тех или иных осложнений со стороны ЖКТ в 2 раза реже в сравнении с другими НПВП. Число спонтанных сообщений о проблемах, связанных с этим препаратом, составило лишь 10,4% от их общего числа. При этом диклофенак был причиной проблем в 21,2%, кетопрофен - 21,7%, а пироксикам - 18,6%.
Опасность развития ЖКТ-кровотечения на фоне приема разных НПВП в реальной клинической практике оценивалась в масштабном эпидемиологическом исследовании J.Laporte и соавт. Исследуемый материал был получен при анализе причин 2813 эпизодов этого осложнения (7193 пациента в качестве контроля). Нимесулид оказался более безопасен, чем многие другие популярные в Европе НПВП: относительный риск кровотечения для нимесулида составил 3,2, для диклофенака - 3,7, мелоксикама - 5,7, рофекоксиба - 7,2.
Большое значение имеет оценка влияния нимесулида на состояние ССС. Следует отметить, что вопрос сравнительного риска развития инфаркта миокарда при использовании нимесулида, по всей видимости, был освящен лишь в одной крупной работе, проведенной финскими учеными. В ходе этого масштабного исследования проанализировано 33 309 эпизодов инфаркта миокарда, при этом контроль по полу и возрасту составили 138 949 лиц. Согласно полученным результатам относительный риск инфаркта для нимесулида - 1,69. Это значение приближалось к соответствующему показателю, определенному для мелоксикама, набуметона, этодолака и неселективных НПВП.
Результаты российских исследований
Нимесулид активно изучался в России. Недавно нами был опубликован обзор российских клинических исследований, в которых определяли сравнительную эффективность и безопасность этого препарата. Всего за период с 1995 по 2009 г. было проведено 21 исследование, в которых нимесулид назначался в дозе от 200 до 400 мг/сут на срок от 7 дней до 12 мес (рис. 2). Нимесулид был использован у 1590 больных, причем помимо пациентов, страдающих РЗ, здесь были и пациенты с острыми травмами, урологической патологией, а также люди, перенесшие стоматологические операции.
Рис. 2. Обзор данных 21 российского клинического исследования, в которых проводилось сравнение нимесулида 200–400 мг/сут (n=1590) и активного контроля (n=526): частота основных побочных эффектов.
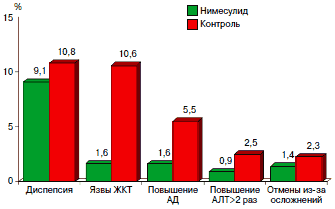
Контроль составили пациенты, которым назначались другие НПВП (в основном диклофенак), парацетамол, трамадол и гомеопатический препарат артрофоон (всего 526 больных). Во всех работах нимесулид не уступал или превосходил препараты сравнения по эффективности: число больных, у которых отмечалось значимое улучшение, составляло от 40 до 90%. В плане безопасности он также показал себя с самой лучшей стороны. Так, число больных с диспепсией при использовании нимесулида составило 9,1%, препаратов сравнения - 10,8%; язвы ЖКТ развились у 1,6 и 10,6% (p<0,001); повышение АД у 1,6 и 5,5% (p<0,001); повышение аланинаминотрансфераз (АЛТ) у 0,9 и 2,5% (p<0,05); потребовались отмены у 1,4 и 2,5% (p<0,05). У единичных больных отмечались отеки и кожные аллергические реакции. В целом, хотя переносимость нимесулида и не была идеальной, она оказалась существенно и достоверно лучше, чем наиболее часто используемого препарата сравнения диклофенака.
В 2009 г. нами была опубликована работа, посвященная изучению развития побочных эффектов при длительном использовании нимесулида. Мы провели ретроспективный анализ частоты осложнений со стороны ЖКТ, кардио-васкулярной системы и печени у 322 больных РЗ, находившихся на стационарном лечении в клинике НИИР РАМН в 2007-2008 гг. и не менее 12 мес до поступления принимавших нимесулид. Всем пациентам была проведены гастроскопия и систематический контроль АД и биохимических показателей крови.
Ни у кого из больных на фоне лечения нимесулидом не развилось опасных осложнений со стороны ЖКТ - таких как кровотечение или перфорации язвы. Язвы желудка и двенадцатиперстной кишки были выявлены у 13,3% обследованных пациентов. Это примерно на 1/3 меньше, чем число язв, возникающих на фоне приема н-НПВП. Так, ранее мы показали, что у 4931 больного, получавшего н-НПВП (преимущественно диклофенак), язвы верхних отделов ЖКТ были выявлены у 18,1% из них.
Несмотря на то что в изучаемой группе был серьезный коморбидный фон по заболеваниям ССС, за 12-месячный предшествующий период инфаркт миокарда был зафиксирован лишь у 1 пациента. Это мужчина 68 лет, страдавший РА, ишемической болезнью сердца в течение многих лет и высокой АГ. Еще у 2 пациенток на фоне приема нимесулида была отмечена отрицательная динамика электрокардиограммы, описанная кардиологом как постинфарктный кардиосклероз.
Стойкое повышение АД в период госпитализации отмечено у 11,5% больных. Среди лиц, исходно имевших эту патологию, частота дестабилизации АГ была существенно выше, чем в целом по группе, и составила 26,8%.
Ни у кого из больных не развилось клинически выраженной патологии печени - желтухи, гепатомегалии, симптомов печеночной недостаточности. Существенное повышение печеночных ферментов (более чем в 2 раза в сравнении с нормой) возникло лишь у 7 (2,2%) больных. Все они страдали РА и помимо нимесулида получали цитотоксические препараты - метотрексат или лефлуномид.
Гепатотоксичность нимесулида
Обсуждая перспективы применения нимесулида, следует обратить особое внимание на проблему осложнений со стороны печени. НПВП-гепатопатия представляет собой проявление метаболической идиосинкразии и возникает редко (в сравнении с другими лекарственными осложнениями). По многолетней статистике серьезные гепатотоксические осложнения, проявляющиеся клинически выраженным внутрипеченочным холестазом или острой печеночной недостаточностью, возникают на фоне регулярного приема НПВП примерно у 1 из 10 тыс. пациентов.
В отношении нимесулида к 2000 г. за 15-летний период (1985-2000 гг.) его применения в 50 разных странах было отмечено лишь 192 случая серьезных осложнений со стороны печени. Учитывая, что на 2000 г. нимесулидом были пролечены 280 млн больных, суммарная частота опасных гепатотоксических реакций составляет менее 1 случая на 1 млн проведенных курсов лечения.
Основной орган Европейского союза, обеспечивающий контроль над оборотом лекарственных препаратов в Европе, - EMEA (European Medicines Agency) после рассмотрения этой проблемы не нашел оснований для прекращения использования нимесулида (пресс-релиз от 21.09.07). Было принято компромиссное решение рекомендовать ограничить применение нимесулида в странах Европы курсом не более 15 дней и в дозе, не превышающей 200 мг/сут. Для исполнения этого решения странам - членам Европейского союза было рекомендовано изъять из аптечной сети упаковки, которые содержат более 30 стандартных доз нимесулида.
Самое важное в этом документе, по мнению C.Mattia и соавт., - признание того факта, что гепатотоксичность нимесулида не превышает гепатотоксичности многих других НПВП, которые успешно используются в клинической практике.
Повторное рассмотрение вопроса о нимесулиде было проведено медицинским руководством Европейского союза 23 июня 2011 г. Новое постановление EMEA подтвердило основные положения, обозначенные в пресс-релизе от 21.09.07: достоинства нимесулида при кратковременном купировании острой боли явно превышают его недостатки, что оправдывает дальнейшее применение препарата.
Действительно, объективный анализ имеющихся литературных данных показывает, что гепатотоксичность нимесулида не выше, чем у многих других представителей класса НПВП. По данным клинических исследований, негативная динамика лабораторных биохимических показателей, свидетельствующая о развитии патологии печени, отмечается при использовании нимесулида с такой же частотой, как и на фоне приема других НПВП. При назначении нимесулида коротким курсом (не более 30 дней) повышение АЛТ в 2 раза и более отмечается лишь у 0,4% больных, а при длительном многомесячном приеме частота подобных изменений не превышает 1,5%.
Очень важные данные о реальной гепатотоксичности нимесулида можно почерпнуть из исследования D.Sanchez-Matienzo и соавт. Обычно эта работа используется в качестве доказательства того факта, что осложнения со стороны печени при использовании нимесулида возникают достоверно чаще в сравнении с другими НПВП, однако при тщательном исследовании представленного материала выводы могут стать совсем иными.
Авторы провели сопоставление частоты осложнений, связанных с приемом разных НПВП. При этом материалом для анализа являлись спонтанные сообщения практикующих врачей, собранные со всего мира Управлением по контролю пищевых продуктов и лекарств в США и Всемирной организацией здравоохранения (ВОЗ). Так, на 2003 г. ВОЗ получила 185 253 таких «сигнала», большинство из которых, естественно, касалось типичных для НПВП осложнений со стороны ЖКТ и ССС. При этом количество сообщений об осложнениях со стороны печени составило для всех НПВП лишь 2,7%.
Для диклофенака эта пропорция была иной: доля сообщений о гепатотоксических реакциях среди всех осложнений, связанных с этим препаратом, выросла до 4,7%. Наименее удачной данная пропорция оказалась для нимесулида - 14,4%. На основании этих цифр, казалось бы, можно сделать вывод, что нимесулид более опасен для печени, чем другие НПВП.
Картина представляется иной, если оценить не относительные, а абсолютные данные по осложнениям со стороны печени. Так, общее количество сообщений о гепатотоксических реакциях при использовании диклофенака составило 990, ибупрофена - 590, а нимесулида - лишь 152. Самое главное, что угрожающая жизни патология - печеночная недостаточность была зафиксирована ВОЗ у 21 больного, получавшего диклофенак, 32 - получавших ибупрофен, и только у 4 использующих нимесулид (!).
Отсюда видно, во-первых, что осложнения со стороны печени при использовании нимесулида возникают крайне редко, а во-вторых, их абсолютное число очень невелико в сравнении с другими популярными НПВП.
Имеется фактически лишь одна масштабная эпидемиологическая работа, в которой изучалась сравнительная гепатотоксичность НПВП, - исследование итальянских ученых G.Traversa и соавт. Они провели анализ частоты гепатотоксических реакций у 397 537 больных за период с 1997 по 2001 г. Суммарная частота осложнений со стороны печени на фоне приема НПВП составила 29,8 на 100 тыс. пациенто-лет. Соответственно, показатель относительного риска гепатотоксических реакций для всех НПВП составил 1,4. Индивидуальная частота серьезных осложнений со стороны печени при использовании нимесулида составила 35,3 на 100 тыс. человеко-лет меньше в сравнении с диклофенаком - 39,2, кеторолаком - 66,8 и ибупрофеном - 44,6.
Для нас очень важен российский опыт применения нимесулида, ведь в нашей стране за последние 15 лет этот препарат был назначен миллионам больных. И тем не менее до настоящего времени в российской медицинской литературе нет ни одного описания тяжелых гепатотоксических реакций, возникших на фоне этого препарата и закончившихся развитием печеночной недостаточности.
Заключение
На сегодняшний день нимесулид представляется одним из наиболее удачных представителей группы НПВП по соотношению эффективности, хорошей переносимости и низкой стоимости, являясь одним из наиболее популярных НПВП в России, Восточной и Центральной Европе.
Основным достоинством нимесулида является сочетание быстрого анальгетического эффекта, хорошего противовоспалительного действия, благоприятной переносимости (в сравнении с «традиционными» НПВП) и низкой стоимости. Риск развития гепатотоксических осложнений при использовании нимесулида не превышает аналогичных показателей для других популярных НПВП (в частности, диклофенака).
В России накоплен большой позитивный опыт применения нимесулида, отражением которого стала серия отечественных контролируемых клинических исследований, где нимесулид показал себя как эффективное и относительно безопасное обезболивающее средство.
В нашей стране нимесулид получили миллионы пациентов, многие из них принимали его в течение длительного времени, и при этом не было зафиксировано ни одного эпизода тяжелых гепатотоксических реакций.
| Июль 2013 г. |