Опубликовано в журнале:
«РОССИЙСКИЙ КАРДИОЛОГИЧЕСКИЙ ЖУРНАЛ»; № 3(101); 2013; стр. 56-62.Коррекция поражений органов-мишеней у больных хронической сердечной недостаточностью ишемической этиологии на фоне терапии ивабрадином
Суровцева М. В., Козиолова Н. А., Чернявина А. И.
ГБОУ ВПО Пермская государственная медицинская академия им. ак. Е. А. Вагнера Минздрава России, Пермь, Россия.Цель.
Оценить возможности ивабрадина в коррекции поражений органов-мишеней у больных ХСН ишемической этиологии в составе комплексной терапии.Материал и методы.
Обследовано 90 больных ХСН II-III функционального класса на фоне стабильной стенокардии. В зависимости от антиишемической терапии пациенты были разделены на 3 группы: 1-я группа - пациенты, получавшие периндоприл и ивабрадин, 2-я группа - получавшие периндоприл, бисопролол и ивабрадин, 3-я группа - пациенты, получавшие периндоприл и бисопролол. Длительность терапии - 6 месяцев. До и после лечения оценивали состояние почек и артерий: скорость клубочковой фильтрации (СКФ) по формуле MDRD, скорость пульсовой волны (СПВ) по сосудам преимущественно эластического типа справа и слева (R-PWV, L-PWV); сердечно-лодыжечно-сосудистый индекс (CAVI1); СПВ в каротидно-феморальном сегменте (PWVcf); СПВ аорты (PWV) и СПВ сонной артерии (C-PWV); индекс усиления систолического АД - индекс аугментации (R-AI - показатель плечевой плетизмограммы, C-AI - показатель сфигмограммы на сонной артерии). В крови определяли уровень N-концевого фрагмента мозгового натрий-уретического пептида (NT-proBNP) и интегральных показателей изменения внеклеточного коллагенового матрикса почек и артерий: тканевого ингибитора матриксных металлопротеиназ (TIMP-1) и С-концевого телопептида проколлагена 1 типа (СТР-1).Результаты.
На фоне 6-месячной комплексной терапии с включением ивабрадина отмечена достоверная положительная динамика СКФ, показателей изменения внеклеточного коллагенового матрикса (TIMP-1 и СТР1) и NT-proBNP как маркера миокардиального стресса. Также отмечено достоверное улучшение структуры и функции артериальной стенки, характеризующееся снижением ее жесткости, оцениваемое по уменьшению CAVI1 и PWVcf, увеличением ее эластичности и растяжимости, что подтверждалось снижением PWV и C-PWV. При сравнении динамики показателей сосудистого ремоделирования в группах с ивабрадином, отмечено достоверно большее улучшение эластичности и растяжимости артерий у пациентов, получавших 3-х компонентную терапию.Выводы.
Результаты применения ивабрадина в комплексной терапии больных ХСН ишемической этиологии показали возможность исследуемого препарата оказывать нефро- и вазопротективное действие.Ключевые слова: хроническая сердечная недостаточность, антиишемическая терапия, коррекция поражений органов-мишеней, ивабрадин.
IVABRADINE THERAPY AND CORRECTION OF THE TARGET ORGAN PATHOLOGY IN PATIENTS WITH ISCHEMIC CHRONIC HEART FAILURE
Surovtseva M. V., Koziolova N. A., Chernyavina A. I.
Academician E. A. Vagner Perm State Medical Academy, Perm, Russia.Aim.
To assess the therapeutic potential of ivabradine, as a part of complex treatment regime, for the correction of the target organ pathology in patients with chronic heart failure (CHF) of ischemic aetiology.Material and methods.
In total, 90 patients with Functional Class II-III CHF and stable angina were examined. All participants were divided into three groups, by the type of 6-month antiischemic therapy: Group 1 received perindopril and ivabradine; Group 2 was administered perindopril, bisoprolol, and ivabradine; and Group 3 received perindopril and bisoprolol. At baseline and after 6 months of the treatment, the following renal and arterial parameters were assessed: glomerular filtration rate (GFR; MDRD formula); pulse wave velocity (PWV measured for elastic-type vessels on the right and left side: R-PVW and L-PVW); cardiac-ankle-vascular index (CAVI1); carotid-femoral PWV (PWVcf); aortic PWV (PWV) and carotid PWV (C-PWV); and radial and carotid augmentation index (R-AI and C-AI). In addition, blood levels of the following biomarkers were measured: N-terminal pro B-type natriuretic peptide (NT-proBNP); and key markers of renal and arterial extracellular collagen matrix: tissue inhibitor of matrix metalloproteinase 1 (TIMP-1) and C-terminal telopeptide of collagen 1 (CTP-1).Results.
After 6 months of a complex ivabradine-including therapy, a significant positive dynamics was observed for the levels of GFR, TIMP-1 and CTP-1 (extracellural collagen matrix markers), and NT-proBNP (a myocardial stress marker). The improvement in arterial wall structure and function was manifested in both reduced stiffness (decreased CAVI1 and PWVcf) and increased elasticity and distensibility (decreased PWV and C-PWV). The improvement in arterial elasticity and distensibility was significantly greater in patients receiving the three-medication therapy.Conclusion.
The findings on the ivabradine therapy, as a part of complex treatment regime in patients with ischemic CHF demonstrated nephro- and vasoprotective effects of ivabradine.Key words: chronic heart failure, ivabradine.
Концепция сердечно-сосудистого континуума, сложившаяся в последние годы, подразумевает непрерывное развитие сердечно-сосудистых заболеваний от факторов риска до развития хронической сердечной недостаточности (ХСН). Неотъемлемыми составляющими континуума являются дисфункция эндотелия и ремоделирование органов-мишеней и, в первую очередь, — миокарда, почек, сосудов. Частота почечной дисфункции при ХСН достаточно велика и зависит от типа кардиоренального синдрома, стабильности течения заболевания, типа дисфункции левого желудочка [1]. Ряд сосудистых маркеров ассоциируется не только с тяжестью, но и с исходами ХСН [2].
Повышенная частота сердечных сокращений (ЧСС) как показатель избыточной симпатической активности рассматривается в настоящее время как в качестве одного из маркеров прогрессирования поражения органов-мишеней у больных ХСН, так и рутинного критерия эффективности лечения [3—5], и является независимым прогностическим фактором [5, 6]. Поэтому в последние годы эффективность бета-адреноблокаторов, как обязательного компонента лечения больных ХСН со сниженной фракцией выброса левого желудочка (ФВЛЖ) и относящегося к группе ЧСС-урежающих препаратов, рассматривается не только с позиций влияния на течение ХСН, но и в плане органопротекции. Обобщенные данные ряда крупных контролируемых исследований показали противоречивые результаты по влиянию бета-адреноблокаторов на регресс почечной дисфункции и функционального состояния артериального русла у больных ХСН и сердечно-сосудистыми заболеваниями [1, 7, 8]. Кроме этого, применение бета-адреноблокаторов у части больных ХСН ограничивается возникновением побочных эффектов или их непереносимостью.
Крупные многоцентровые исследования BEAUTIFUL (morBidity-mortality EvAlUaTion of the If inhibitor ivabradine in patients with coronary artery disease and left ventricULar systolic dysfunction), SHIFT ((the Systolic Heart Failure Treatment with the I (f) Inhibitor Ivabradine Trial)) показали возможности лечения больных ХСН ивабрадином — селективным ингибитором If-каналов клеток синусового узла, урежающим ЧСС [9, 10]. Данные о влиянии ивабрадина на состояние фильтрационной функции почек у больных ХСН отсутствуют. В экспериментальных исследованиях на животных было найдено, что ивабрадин обладает дозозависимым нефропротективным эффектом при индуцировании ренальной ишемии [11].
В литературе также описаны клинические случаи успешного применения ивабрадина у больных хронической почечной недостаточностью после трансплантации сердца [12].
Действие ивабрадина на жесткость сосудистой стенки неизвестно. В экспериментальных работах на мышах было найдено, что снижение ЧСС на фоне использования ивабрадина обеспечивает уменьшение сосудистой жесткости за счет участия в регуляции функционирования ангиотензиновых рецепторов 1 типа, подавления оксидативного стресса и модуляции экспрессии провоспалительных цитокинов [13].
Следовательно, поиск новых ЧСС- урежающих препаратов и оценка их влияния на органы-мишени, скомпрометированные при ХСН, является актуальной перспективной кардиологической задачей, требующей проведения дальнейших исследований.
Цель исследования — оценить возможности ивабрадина в коррекции поражений органов-мишеней (почки, артерии) у больных ХСН ишемической этиологии в составе комплексной терапии.
Материал и методы
Проведено сравнительное рандомизированное клиническое исследование. Обследовано 205 пациентов стабильной стенокардией II—III функционального класса (ФК). Из них выделена когорта больных с ХСН II—III ФК — 90 человек. Средний возраст больных составил 56,2±6,4 лет, среди них 58,8% (53) мужчин, 41,1% (37) женщин. Продолжительность стенокардии среди обследованных составила 5,9±2,6 года, средний ФК составил 2,27±0,37. Инфаркт миокарда в анамнезе выявлен у 37,7% (34) больных. Продолжительность ХСН — 6,2±2,1 лет. Средний ФК ХСН составил 2,52±0,08. Критериями включения в исследование являлись: возраст от 30 до 65 лет; наличие стабильной стенокардии II—III ФК, подтвержденной клинически и/или нагрузочными тестами; наличие ХСН II—III ФК, подтвержденной наличием клинических признаков и дисфункции миокарда левого желудочка по данным эхокардиографии (ЭхоКГ) или увеличением уровня N-концевого фрагмента мозгового натрий-уретического пептида (NT-proBNP); синусовый ритм на ЭКГ; получение информированного согласия на участие в исследовании. Критериями исключения из исследования были следующие: острый коронарный синдром; ХСН неишемической этиологии; вторичная стенокардия; митральный стеноз; митральная и аортальная регургитация более II степени; онкологические заболевания; острые воспалительные и инфекционные заболевания; противопоказания к назначению ингибиторов ангиотензинпревращающего фермента (ИАПФ), бета-адреноблокаторов и ивабрадина; деменция и психические заболевания, препятствующие подписанию информированного согласия и дальнейшему адекватному контакту с больным в период наблюдения; иные причины, препятствующие дальнейшему контакту с больным в период наблюдения.Методом простой рандомизации в зависимости от выбора терапии пациенты были разделены на 3 группы по 30 человек: первая группа — пациенты, получавшие в комплексной терапии периндоприл (средняя доза — 5,9±1,8 мг в сутки), ивабрадин (средняя доза — 11,6±1,9 мг в сутки), вторая группа — получавшие периндоприл (средняя доза — 5,7±1,6 мг в сутки), бисопролол (средняя доза — 7,9±1,9 мг в сутки) и ивабрадин (средняя доза — 6,4±1,6 мг в сутки), третья группа — пациенты, получавшие периндоприл (средняя доза — 4,4±1,5 мг в сутки) и бисопролол (средняя доза — 7,2±1,6 мг в сутки). Достоверных различий между группами по использованию статинов, антиагрегантов, ситуационному использованию короткодействующих нитратов и других препаратов для лечения ХСН и стенокардии не было выявлено. Длительность лечения составила 6 месяцев. Для выявления особенностей ремоделирования артериальной стенки всем пациентам проводилась объемная сфигмоплетизмография на приборе VaSera VS-1000 (Fucuda Denshi, Япония). Оценивались следующие показатели: скорость пульсовой волны (СПВ) по сосудам преимущественно эластического типа справа и слева (R-PWV, L-PWV); сердечно-лодыжечно-сосудистый индекс (CAVI1); СПВ в каротидно-феморальном сегменте (PWVcf); СПВ аорты (PWV) и СПВ сонной артерии (C-PWV); индекс усиления систолического АД — индекс аугментации (R-AI — показатель плечевой плетизмограммы, C-AI — показатель сфигмограммы на сонной артерии). В крови определяли уровень интегральных показателей изменения внеклеточного коллагенового матрикса почек и артерий: методом иммуноферментного анализа оценивался уровень С-концевого телопептида проколлагена 1 типа (СТР-1) с помощью наборов “Nordic Bioscience Diagnostics’ (Дания) и тканевого ингибитора матриксных металлопротеиназ I типа (TIMP-1) с помощью наборов “Bio Source EUROPE S.A.” (Бельгия) на анализаторе Stat Fax 303 Plus (Awareness Technology, США). Референсные значения TIMP-1 составляли 111—138 нг/мл, СТР-1 (у мужчин) — 0,115—0,748 нг/мл, у фертильных женщин — 0,112—0,738, у женщин в постменопаузе — 0,142—1,351 нг/мл. Для оценки почечной функции определялись уровень креатинина в сыворотке крови и рассчитывалась скорость клубочковой фильтрации (СКФ) по формуле MDRD (The Modification of Diet in Renal Disease Study, 1996).
Уровень NT-концевого фрагмента мозгового NT-proBNP определялся в сыворотке крови методом хемифлюоресцентного анализа с применением реактива “Hoffman la Roche” (Швейцария) на хемилюминесцентном анализаторе Immulite 1000 (DPC, США).
Статистическую обработку полученных результатов осуществляли при помощи программы STATISTICA 6.0. Для количественных признаков были рассчитаны среднеарифметическое значение (M) и среднеквадратичное отклонение среднего (M±sd); медианы и нижнего и верхнего квартилей (Ме [LQ; UQ]). Для качественных признаков были рассчитаны: абсолютная частота проявления признака (количество обследованных), частота проявления признака в процентах. Анализ вида распределения осуществлен с использованием критерия Шапиро-Уилка. Для ряда данных гипотеза о нормальности распределения была отвергнута. Для статистического сравнительного анализа данных трех групп при нормальном распределении использовали параметрические методы: для количественных показателей — однофакторный дисперсионный анализ (ANOVA), для качественных показателей — критерий 2. Критический уровень достоверности нулевой статистической гипотезы, свидетельствующий об отсутствии значимых различий, принимали равным <0,05. Сравнение трех групп при ненормальном распределении по количественному показателю было проведено с помощью критерия Краскела-Уоллиса с поправкой Бонферрони р/3, по качественному признаку — при помощи критерия 2. Критический уровень достоверности нулевой статистической гипотезы, свидетельствующий об отсутствии значимых различий или факторных влияний, принимали равным ≤0,017.
Результаты
Сравнительная клинико-анамнестическая характеристика больных по группам обследуемых представлена в таблице 1. Группы были сопоставимы по полу, возрасту, факторам риска ИБС, тяжести стенокардии и ХСН, структуре и тяжести сопутствующих заболеваний.Таблица 1
Сравнительная клинико-анамнестическая характеристика обследуемых больных по группам до лечения (n=90)
Показатель 1 группа (n=30) 2 группа (n=30) 3 группа (n=30) р1-2 р2-3 р1-3 рmg Возраст, лет 55,7±4,8 54,9±5,6 57,5±4,8 0,555 0,058 0,152 0,134 Пол, муж, абс. % 21/70,0 18/60,0 14/46,6 0,866 0,724 0,466 0,640 Стаж стенокардии, лет 6,2 (2,4;8,9) 6,6 (2,8;10,5) 6,4 (2,1;11,8) 0,456 0,723 0,748 0,784 Стаж ХСН, лет 6,6 (3,1;12,6) 6,8 (4,5;10,0) 6,7 (4,8;8,9) 0,720 0,851 0,854 0,934 ИМ в анамнезе, абс. % 12/40,0 13/43,3 9/30,0 0,944 0,631 0,756 0,753 ФК стенокардии 2,2 (1,8;2,6) 2,3 (1,9;2,7) 2,3 (1,8;2,7) 0,278 0,772 0,446 0,563 ФК ХСН 2,4 (2,0;2,6) 2,5 (2,1;2,7) 2,5 (2,0;2,7) 0,645 0,701 0,723 0,686 NT-proBNP, пг/мл 889,4 (523,5;1157,7) 852,9 (587,4;1234,9)
884,5 (456,8;1302,0) 0,376 0,513 0,912 0,673 Частота курения - n, % 12/40,0 10/33,3 7/23,3 0,908 0,713 0,461 0,604 ИМТ, кг/м2 32,1±9,8 30,5±11,1 29,2±10,7 0,556 0,646 0,278 0,568 Общий холестерин, ммоль/л 6,2+1,6 6,4+1,8 6,3+1,5 0,651 0,816 0,804 0,781 Наследственность по ИБС - n, % 16/53,3 12/40,0 15/50,0 0,692 0,804 0,940 0,817 СД 2 типа - n, % 1/3,4 2/6,7 1/3,4 0,978 0,978 0,472 0,789 АГ - n, % 28/93,3 27/90,0 25/83,3 0,929 0,839 0,764 0,812 ХОБЛ - n, % 3/10,0 4/13,3 2/6,7 0,967 0,726 0,971 0,846 Атеросклероз артерий нижних конечностей - n, % 2/6,7 3/10,0 2/6,7 0,971 0,971 0,606 0,788 Атеросклероз сонных артерий - n, % 1/3,3 3/10,0 2/6,6 0,651 0,971 0,978 0,625 Сокращения: ИМ - инфаркт миокарда, ИМТ - индекс массы тела, СД - сахарный диабет, АГ - артериальная гипертония, ХОБЛ - хроническая обструктивная болезнь легких, pmg (p multigroup) - критерий множественного межгруппового сравнения.Достоверных различий между группами по структуре и тяжести поражения органов-мишеней до лечения найдено не было (табл. 2).
Таблица 2
Сравнительная характеристика показателей поражения органов-мишеней у обследуемых больных по группам (n=90)
Показатель 1 группа (n=30) 2 группа (n=30) 3 группа (n=30) р1-2 р2-3 р1-3 рmg СКФ, мл/мин/1,73м 51,67±6,12 51,33±5,35 50,57±6,72 0,820 0,630 0,510 0,684 R-PWV, м/с 14,98±2,57 13,88±1,99 14,53±1,79 0,069 0,189 0,435 0,223 L-PWV, м/с 14,63±2,36 14,04±2,42 14,33±1,74 0,343 0,596 0,577 0,492 CAVI1 8,98±1,58 8,71±1,65 8,61±1,16 0,520 0,787 0,305 0,486 PWVcf, м/с 11,40±2,10 11,50±1,10 12,0±1,30 0,818 0,113 0,189 0,285 PWV, м/с 6,96±2,24 6,84±3,14 5,91±2,17 0,865 0,187 0,070 0,236 C-PWV, м/с 0,51±0,12 0,48±0,19 0,49±0,11 0,468 0,804 0,504 0,674 С-AI 1,35±0,78 1,29±0,52 1,15±0,37 0,727 0,234 0,210 0,326 R-AI 1,19±0,24 1,25±0,27 1,32±0,29 0,367 0,337 0,064 0,127 CTP-1, нг/мл 0,44±0,18 0,50±0,24 0,49±0,20 0,278 0,861 0,313 0,492 TIMP-1, нг/мл 172,3±89,8 203,4±58,6 187,3±76,8 0,118 0,365 0,490 0,291 Сокращения: pmg (p multigroup) - критерий множественного межгруппового сравнения.В течение всего периода наблюдения исследуемые препараты хорошо переносились пациентами, отмены лекарственных средств не потребовалось. Средние дозы исследуемых препаратов к концу исследования составили: в первой группе периндоприл — 5,2±1,8 мг, ивабрадин — 11,6±1,9 мг; во второй группе периндоприл — 5,1±1,6 мг, бисопролол — 3,1±1,9 мг, ивабрадин — 11,4±1,6 мг; в третьей группе периндоприл — 4,4±1,5 мг, бисопролол — 3,9±2,1 мг.
Динамика течения ХСН в течение 6 месяцев терапии представлена в таблице 3.
Таблица 3
Динамика течения хронической сердечной недостаточности на фоне лечения по группам обследуемых (n=90)
Параметр, Δ% 1 группа
(n=30)2 группа
(n=30)3 группа
(n=30)р1-2 р2-3 р1-3 рmg Δ ЧСС -8,9±2,5 -10,5±3,2 -5,3±4,1 0,005 <0,001 <0,001 <0,001 Δ теста 6-минутной ходьбы 7,76±4,88 6,72±2,05 4,61±3,33 0,286 0,005 0,005 0,014 Δ NT-proBNP -18,15±15,97 -11,67±10,49 -1,67±4,98 0,068 <0,001 <0,001 <0,001 Сокращения: pmg (p multigroup) - критерий множественного межгруппового сравнения.При сравнении групп пациенты по динамике баллов по ШОКС достоверно не различались (р =0,483).
Достоверных различий между группами в ходе исследования по динамике сывороточного креатинина не было выявлено. Через 6 месяцев лечения СКФ увеличилась достоверно больше во второй группе больных по сравнению с первой и третьей группами (р1-3<0,001; р2-3<0,001; рmg =0,014). Первая и вторая группы по динамике СКФ после лечения достоверно не различались (р =0,052) (рис. 1).
Рис. 1. Динамика СКФ у больных ХСН ишемической этиологии после лечения.
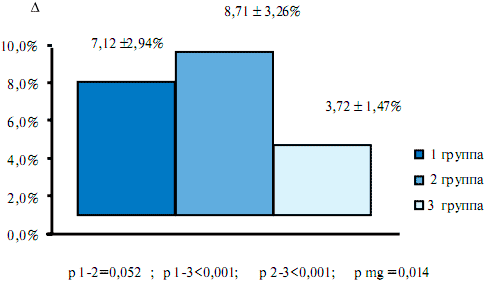
В таблице 4 представлена динамика показателей объемной сфигмоплетизмографии по группам обследуемых. Как видно из таблицы, на фоне лечения отмечено достоверное снижение R-PWV и L-PWV во второй и первой группах, в то время как в группе больных, получавших периндоприл и бисопролол, эти показатели, напротив, увеличились (р1-3<0,001 р <0,001, рmg <0,001). Группы с включением ивабрадина с комплексную терапию по динамике R-PWV и L-PWV значимо не различались (р =0,375 и 0,172 соответственно).
Таблица 4
Динамика показателей объемной сфигмоплетизмографии на фоне терапии по группам обследуемых (n=90)
Параметр, Δ% 1 группа (n=30) 2 группа (n=30) 3 группа (n=30) р1-2 р2-3 р1-3 рmg R-PWV -9,58
(-13,21;-2,46)-7,91
(-12,57;-4,85)5,51
(0,99;9,25)0,375 <0,001 <0,001 <0,001 L-PWV -6,66
(-12,05;-4,08)-8,50
(-13,40;-2,21)5,49
(1,65;10,65)0,172 <0,001 <0,001 <0,001 CAVI1 -7,41
(-15,97;-4,08)-15,22
(-22,57;-8,43)-6,14
(-7,75;-4,70)0,018 <0,001 0,015 <0,001 PWVcf -21,29
(-27,07;-15,07)-21,51
(-28,80;-8,25)-14,20
(-24,06;-5,28)0,524 <0,001 <0,001 <0,001 PWV -11,70
(-21,23;-4,32)-22,03
(-33,38;-16,39)1,89
(-4,41;8,18)0,010 <0,001 <0,001 <0,001 C-PWV -10,11
(-1,51;-6,52)-24,15
(-28,57;-16,12)1,28
(0,81;1,70)0,001 <0,001 <0,001 <0,001 С-AI -21,28
(-27,09;-14,10)-9,38
(-14,26;-5,26)2,64
(-0,41;3,48)0,002 <0,001 <0,001 <0,001 R-AI -19,19
(-24,89;-13,09)-19,55
(-28,46;-6,58)-9,55
(-22,25;0,99)0,125 <0,001 <0,001 <0,001 Сокращения: pmg (p multigroup) - критерий множественного межгруппового сравнения.Через 6 месяцев лечения в группе больных, получавших периндоприл, бисопролол и ивабрадин, индекс CAVI1 снизился достоверно больше, чем в первой и третьей группах (р <0,001). При оценке динамики СПВ в каротидно-феморальном сегменте получены аналогичные различия (р <0,001), однако первая и вторая группы достоверно не отличались (р1-2=0,524).
На фоне 6-месячной комплексной терапии отмечена достоверно большая положительная динамика СПВ в аорте и сонной артерии во второй группе больных по сравнению с первой и третьей группами (р <0,001). Индекс аугментации C-AI после лечения снизился достоверно больше в группе больных, получавших периндоприл и ивабрадин, чем в группе во второй и третьей группах (р <0,001). При оценке динамики индекса аугментации R-AI получены аналогичные различия, при этом первая и вторая группы достоверно не отличались (р =0,125).
TIMP-1 достоверно уменьшился во второй и первой группах, в третьей группе изменился недостоверно (р1-2=0,854, р2-3 <0,001, р1-3, <0,001, рmg <0,001). СТР-I во второй группе увеличился достоверно больше, чем в первой группе (р =0,011). В третьей группе обнаружено негативное достоверное уменьшение уровня СТР-1 после лечения (р <0,001, р1-3<0,001, рmg<0,001).
Анализ динамики уровня NT-proBNP выявил его достоверное уменьшение в первой и во второй группах по сравнению с третьей группой. Первая и вторая группа по динамике NT-proBNP достоверных различий не имели (р1-2=0,901, р2-3<0,001, р1-3<0,001, рmg<0,001) (табл. 5).
Таблица 5
Динамика показателей эндогенного коллагенолиза и маркера миокардиального стресса на фоне терапии по группам обследуемых (n=90)
Параметр, Δ% 1 группа
(n=30)2 группа
(n=30)3 группа
(n=30)р1-2 р2-3 р1-3 рmg TIMP-1 -17,50±3,87 -17,65±2,18 3,37±1,44 0,854 <0,001 <0,001 <0,001 СТР-I 18,92±3,51 21,49±4,06 -2,92±1,31 0,011 <0,001 <0,001 <0,001 NT-proBNP -18,15±7,38 -17,92±6,85 -3,49±1,46 0,901 <0,001 <0,001 <0,001 Сокращения: pmg (p multigroup) - критерий множественного межгруппового сравнения.Обсуждение
Нарушение функции почек наблюдалось у 45—63,6% больных ХСН, что свидетельствует о формировании кардиоренального синдрома (КРС) 2-го типа [14, 15], значительно повышающего риск общей и сердечно-сосудистой смертности [16, 17, 18]. Основными патогенетическими звеньями КРС у больных ХСН считают снижение сердечного выброса, активацию нейрогуморальных систем, воспаление и оксидативный стресс, что приводит к формированию порочного круга, ускоряющего снижение функциональной способности каждого из органов и прогрессирование ремоделирования миокарда, почек, сосудов [19]. Нейрогуморальные медиаторы — ангиотензин II, катехоламины, эндотелин-1 играют огромную роль как в ремоделировании почечной ткани, так и в ремоделировании артерий, оказывая не только вазоактивное, но и гипертрофическое, профибротическое влияние [20, 21]. Избыток оксидантов способствует пролиферации гладкомышечных клеток, утолщению медиального слоя сосудистой стенки, нарушению состава внеклеточного матрикса и структуры артериальной стенки в целом [22].Результаты нашей работы показали, что включение ивабрадина в комплексную терапию больных ХСН ишемической этиологии сопровождается достоверной положительной динамикой СКФ, показателей изменения внеклеточного коллагенового матрикса (TIMP-1 и СТР-1) и NT-proBNP как маркера миокардиального стресса. Также отмечено достоверное улучшение структуры и функции артериальной стенки, характеризующееся снижением ее жесткости, оцениваемое по уменьшению CAVI1 и PWVcf, увеличением ее эластичности и растяжимости, что подтверждалось снижением PWV и C-PWV. При сравнении динамики показателей сосудистого ремоделирования в группах с ивабрадином отмечено достоверно большее улучшение эластичности и растяжимости артерий у пациентов, получавших 3-х компонентную терапию с включением ивабрадина.
Возможные механизмы вазо- и нефропротективного эффектов ивабрадина представлены в ряде экспериментальных исследований на животных. Так P. Millez et al. показали, что ивабрадин препятствует ухудшению анатомического и электрического ремоделирования сердца у крыс с постинфарктной сердечной недостаточностью. При этом было отмечено, что подобное действие ивабрадина связано, скорее всего, с регуляцией РААС, поскольку было найдено, что ивабрадин уменьшает количество коллагена в миокарде, экспрессию АПФ и ангиотензиновых рецепторов 1 типа к ангиотензину II [23]. В данной работе также было определено, что ивабрадин изменяет коллагенообразование в миокарде у крыс с постинфарктной сердечной недостаточностью за счет увеличения плотности капилляров [24]. P. Becher et al. в эксперименте установили, что у крыс с ангиотензин II — индуцированной сердечной недостаточностью ивабрадин, в отличие от метопролола, достоверно улучшал систолическую и диастолическую функцию левого желудочка за счет регресса гипертрофии, фиброза, воспаления и апоптоза миокарда, возможно и гладкомышечных клеток сосудов [25]. В исследованиях на животных получены плейотропные эффекты ивабрадина — такие, как антиоксидантный, антиатеросклеротический, улучшение эндотелиальной дисфункции. Так в работе F. Custodis et al. установлено, что снижение ЧСС с помощью 6-недельного применения ивабрадина уменьшает выработку маркеров оксидативного стресса, улучшает функцию эндотелия и уменьшает размеры атеросклеротической бляшки у мышей независимо от АД и уровня липидов [26]. M. Baumh kel et al. показали, что у мышей на фоне эндотелиальной дисфункции, индуцированной диетой с высоким содержанием холестерина, 3-месячная терапия ивабрадином способствует уменьшению размеров атеросклеротических бляшек и улучшению эндотелиальной дисфункции [27]. A. Dominguez-Rodriguez et al. также отметили при применении ивабрадина уменьшение размеров атеросклеротических бляшек у экспериментальных животных на фоне липид-индуцированного атеросклероза [28]. A. Drouin et al. выявили, что после 3-месячной терапии ивабрадином у мышей с дислипидемией на фоне снижения ЧСС уменьшается эндотелиальная дисфункция сосудов эластического типа [29]. A. Beytur et al. обнаружили дозозависимый положительный эффект ивабрадина у крыс с ишемическим повреждением почек, проявляющийся снижением уровня креатинина, азота мочевины, тканевого малонового диальдегида, а также повышением уровня каталазы и супероксиддисмутазы в почечной ткани [11].
Следовательно, можно предположить, что положительное влияние ивабрадина на функцию почек и артериальную стенку у больных ХСН, отмеченное в нашей работе, связано как со способностью ивабрадина обеспечивать профилактику интерстициального фиброза, что было найдено в исследовании, так и с влиянием его на нейрогуморальные механизмы — в частности, на РААС, симпатическую нервную систему, оксидативный стресс, апоптоз, воспаление.
Заключение
Результаты применения ивабрадина в комплексной терапии больных ХСН ишемической этиологии показали возможность исследуемого препарата оказывать нефропротективное и вазопротективное действие, что сопровождалось достоверной положительной динамикой СКФ, показателей структуры и функции артериальной стенки по данным объемной сфигмоплетизмографии. Профилактика фиброза внеклеточного коллагенового матрикса почек и артерий явилась, по данным нашей работы, одним из механизмов регресса почечной дисфункции и артериального ремоделирования у больных ХСН ишемической этиологии на фоне действия ивабрадина.Суровцева М. В. - к. м.н., доцент кафедры внутренних болезней педиатрического и стоматологического факультетов, Козиолова Н. А.* - д. м.н., профессор, заведующая кафедрой внутренних болезней педиатрического и стоматологического факультетов, Чернявина А. И. - к. м.н., ассистент кафедры внутренних болезней педиатрического и стоматологического факультетов.
ЛИТЕРАТУРА
1. Cruz D. N., Schmidt-Ott K. M., Vescovo G. et al. Pathophysiology of Cardiorenal Syndrome Type 2 in Stable Chronic Heart Failure: Workgroup Statements from the Eleventh Consensus Conference of the Acute Dialysis Quality Initiative (ADQI). Contrib Nephrol. 2013; 182:117-36.
2. Ky B., French B., Ruparel K. et al. The vascular marker soluble fms-like tyrosine kinase 1 is associated with disease severity and adverse outcomes in chronic heart failure. J Am Coll Cardiol. 2011;58 (4):386-94.
3. Воhm M., Reil J. C., Danchin N. et al. Association of heart rate with microalbuminuria in cardiovascular risk patients: data from I-SEARCH. J Hypertens. 2008; 26 (1):18-25.
4. Jae S. Y, Carnethon M. R., Heffernan K. S. et al. Slow heart rate recovery after exercise is associated with carotid atherosclerosis. Atherosclerosis. 2008; 196 (1):256-61.
5. Goldberger J. J., Cain M. E., Hohnloser S. H. еt al. American Heart Association/American College of Cardiology Foundation/Heart Rhythm Society Scientific Statement on Noninvasive Risk Stratification Techniques for Identifying Patients at Risk for Sudden Cardiac Death. А scientific statement from the American Heart Association Council on Clinical Cardiology Committee on Electrocardiography and Arrhythmias and Council on Epidemiology and Prevention. Circulation. 2008; 118 (14):1497-518.
6. Swedberg K., Komajda М. The beat goes on: on the importance of heart rate in chronic heart failure. Eur Heart J. 2012; 33 (9):1044-5.
7. Chang T. I., Yang J., Freeman J. V. et al. Effectiveness of -blockers in heart failure with left ventricular systolic dysfunction and chronic kidney disease. J Card Fail. 2013; 19 (3):176-82.
8. Tropeano A. I., Saleh N., Hawajri N. et al. Do all antihypertensive drugs improve carotid intima-media thickness? A network meta-analysis of randomized controlled trials. Fundam Clin Pharmacol. 2011; 25 (3):395-404.
9. Bruguera Cortada J., Varela A. Role of heart rate in cardiovascular diseases: how the results of the BEAUTIFUL study change clinical practice. Am J Cardiovasc Drugs 2009; 9 (Supp.l):9-12.
10. Swedberg K., Komajda M., Behm M. et al. Ivabradine and outcomes in chronic heart failure (SHIFT): a randomised placebo-controlled study. Lancet 2010; 376 (9744):875-85.
11. Beytur A., Binbay M, Sarihan M. E. et al. Dose-dependent protective effect of ivabradine against ischemia-reperfusion-induced renal injury in rats. Kidney Blood Press Res.2012; 35 (2):114-9.
12. Kurpesa M., Trzos E., Wierzbowska-Drabik K. et al. Ivabradine as a heart rate-lowering agent in a patient with end-stage renal failure after heart transplantation. Kardiol Pol. 2010; 68 (6):684-6.
13. Custodis F., Fries P., M ller A. et al. Heart rate reduction by ivabradine improves aortic compliance in apolipoprotein E-deficient mice. J Vasc Res. 2012; 49 (5):432-40.
14. Ahmed A., Rich M. W., Sanders P. W. et al. Chronic kidney disease associated mortality in diastolic versus systolic heart failure: a propensity matched
15. study. Am J Cardiol. 2007; 99:393-8.
16. Campbell R. C., Sui S., Filippatos G. et al. Association of chronic kidney disease with outcomes in chronic heart failure: a propensity-matched study. Nephrol Dial Transplant 2009; 24:186-93.
17. Ronco C., McCullough P., Anker S. D. et al. Cardio-renal syndromes report from consensus conference of acute dialysis quality initiative. Eur. Heart J. 2010; 31 (6):703-11.
18. ADQI 7: the clinical management of the cardio-renal syndromes work group statements from the 7th ADQI consensus conference. Nephrol Dial Transplant. 2010; 25 (7):2077-89.
19. Damman K., Navis G., Voors A. A. et al. Worsening renal function and prognosis in heart failure: systematic review and meta-analysis. J Card Fail 2007; 13 (8): 599-608.
20. Кобалава Ж. Д., Ефремовцева М. А., Виллевальде С. В. Кардиоренальные синдромы. Клиническая нефрология 2011; 6:9-15.
21. Lyall F., Morton J. J., Lever A. F., Cragoe E. J. Angiotensin II activates Na-H exchange and stimulates growth in vascular smooth muscle cells. J Hypertens 1988; 6; (14):438-41.
22. Мухин Н. А., Фомин В. В, Моисеев С. В., Хамхоева М. С. Хроническая сердечная недостаточность и поражение почек: перспективы лечения. Consilium Medicum 2008; 10 (9):69-74.
23. Irani K. Oxidant signaling in vascular cell growth, death and survival. Circ Res 2000; 87:179-90.
24. Milliez P. Beneficial effects of delayed ivabradine treatment on cardiac anatomical and electrical remodeling in rat severe chronic heart failure. Am J Physiol Heart Circ Physiol 2009; 296:435-41.
25. Mulder P., Barbier S., Chagraoui A. et al. Long-term heart rate reduction induced by the selective I (f) current inhibitor ivabradine improves left ventricular function and intrinsic myocardial structure in congestive heart failure. Circulation. 2004; 109 (13):1674-79.
26. Becher P. M., Lindner D., Miteva K. et al. Role of heart rate reduction in the prevention of experimental heart failure: comparison between If-channel blockade and -receptor blockade. Hypertension 2012; 59 (5):949-57.
27. Custodis F., Baumh kel M., Schlimmer N. et al. Heart rate reduction by ivabradine reduces oxidative stress, improves endothelial function, and prevents atherosclerosis in apolipoprotein E-deficient mice. Circulation 2008; 117: 2377-87.
28. Baumh kel M., Custodis F., Schlimmer N. et al. Heart rate reduction with ivabradine improves erectile dysfunction in parallel to decrease in atherosclerotic plaque load in ApoE-knockout mice. Atherosclerosis 2010; 212:55-62.
29. Dominguez-Rodriguez A., Blanco-Palacios G., Abreu-Gonzalez P. Increased heart rate and atherosclerosis: potential implications of ivabradine therapy. World J Cardiol. 2011; 3 (4):101-4.
30. Drouin A., Gendron M. E., Thorin E. et al. Chronic heart rate reduction by ivabradine prevents endothelial dysfunction in dyslipidaemic mice. Br J Pharmacol. 2008; 154 (4):749-57.
| Февраль 2014 г. |