Опубликовано в журнале:
«Сахарный диабет», 2011, №3, с. 90-96Результаты открытой наблюдательной программы DIAMOND
Шестакова М.В., Викулова О.К.
ФГУ Эндокринологический научный центр, Москва (директор – академик РАН и РАМН И.И. Дедов)Цель. DIAMOND (DIAMicrON MR in Daily practice) – наблюдательная программа по оценке эффективности и безопасности терапии Диабетоном МВ в повседневной клинической практике.
Материалы и методы. В исследование были включены 394 пациента с неудовлетворительным контролем сахарного диабета 2 типа (СД2) на терапии диетой или одним пероральным сахароснижающим препаратом (ПССП), которые переводились на Диабетон МВ с продолжением или отменой предшествующей терапии (если ранее пациент принимал препарат из группы секретагогов).
Результаты. Через 6 месяцев лечения Диабетоном МВ (в монотерапии у 30% или комбинации у 70% пациентов) целевой уровень HbA1c<7% достигнут у 64,7% пациентов, из них HbA1c<6,5% – у 30,71% пациентов. Отмечалось достоверное снижение массы тела, уровня систолического и диастолического АД, уровня альбуминурии (АУ), а также количества пациентов с микроальбуминурией (МАУ) с 29,19% до 22,59% и протеинурией (ПУ) с 5,08% до 3,30%. Тяжелых гипогликемий отмечено не было, легкие гипогликемии зарегистрированы у 2,28% пациентов.
Выводы. Диабетон МВ показал высокую сахароснижающую эффективность и хорошую переносимость терапии с низким риском гипогликемий и полным отсутствием серьезных нежелательных явлений в условиях повседневной клинической практики. На фоне улучшения контроля гликемии отмечены нефропротективные эффекты.
Ключевые слова: сахарный диабет 2 типа, гипогликемия, Диабетон МВ, исследование ADVANCE.
The results of open observational trial DIAMOND
Shestakova M.V., Vikulova O.K.
Endocrinological Research Centre, MoscowAim. DIAMOND (DIAMicrON in Daily practice) is an open non-randomized observational trial aimed to estimate the efficacy and safety of gliclazide (Diamicron MB) in routine clinical practice.
Materials and methods. 394 patients with poor control of type 2 diabetes mellitus (T2 DM), previously treated with diet or one of oral antidiabetic drug (OAD), were switched to Diamicron MB. Previous therapy was left unchanged, except for a sulfonylurea or glinide that were canceled.
Results. After 6 months of Diamicron MB therapy (30% monotherapy, 70% combined therapy) target HbA1c<7% was reached in 64,7% of patients, HbA1c<6,5% in 30,71% patients. Statistically significant reduction of body weight, systolic and diastolic blood pressure, microalbuminuria rate was reached. The number of patients with microalbuminuria decreased from 29,19% to 22,59%, with proteinuria from 5,08% to 3,30%. No severe hypoglycemia was registered, light hypoglycemia was seen in 2,28% of patients.
Conclusions. Diamicron MB was effective and well-tolerated and showed low risk of hypoglycemia with no severe adverse effects in daily routine practice. Diamicron MB demonstrated nephroprotective features as a result of better glycemic control.
Key words: type 2 diabetes mellitus, hypoglycemia, Diamicron MB, ADVANCE trial.
Вследствие многообразия механизмов, участвующих в развитии нарушений углеводного обмена при сахарном диабете 2 типа (СД2), спектр возможных терапевтических воздействий также достаточно широк. Дисфункция β-клеток – один из ключевых патофизиологических механизмов развития и прогрессирования СД2. Дефект секреции инсулина обязательно присутствует практически у всех пациентов СД2, и с этой точки зрения секретагоги абсолютно востребованы в качестве патогенетической терапии. Несмо- тря на появление новых классов сахароснижающих средств, влияющих на секрецию инсулина, производные сульфонилмочевины (СМ) остаются наиболее часто назначаемыми пре- паратами в реальной клинической практике. Так, по данным исследования ДИА-контроль по оценке диабетологической ситуации в различных регионах РФ, включившего более 5 тысяч пациентов с СД2, препараты СМ занимают до 54% в структуре сахароснижающей терапии [1]. Причины столь частого назначения СМ заключаются не только в экономической доступности, но в немалой степени обусловлены самой высокой среди ПССП сахароснижающей эффективностью, предсказуемыми эффектами и длительным опытом успешного применения.
Традиционно с препаратами СМ связывают наиболее высокий риск таких побочных эффектов, как гипогликемии и повышение веса. Однако, пожалуй, ни один другой класс ПССП не обладает столь выраженными различиями характеристик препаратов внутри класса [2]. Особенности фармакокинетики, различное сродство, селективность и обратимость рецепторного взаимодействия обусловливают значимые отличия в свойствах различных представителей СМ и, в первую очередь, профиле безопасности [3–5].
Гликлазид МВ (Диабетон® MR) – препарат СМ 2-й генерации – обладает целым спектром положительных качеств, которые обеспечивают оптимальную переносимость препарата [2]. Обратимость связывания гликлазида МВ с рецептором, восстановление физиологической секреции инсулина, образование неактивных метаболитов способствуют меньшему риску развития гипогликемий (табл. 1). Оптимальная переносимость и безопасность гликлазида МВ подтверждены данными многих клинических исследований [3, 6, 7].
Таблица 1. Свойства гликлазида, способствующие меньшему риску развития гипогликемий
Для гликлазида МВ, в отличие от глибенкламида и глимепирида, характерна высокая обратимость связывания с рецептором β-клеток. Это позволяет избежать длительной стимуляции секреции и развития гиперинсулинемии, а следовательно: снижает риск гипогликемий и увеличение веса – с одной стороны, истощение β-клеток и развитие резистентности к действию препарата – с другой Гликлазид МВ, в отличие от глибенкламида, способствует восстановлению раннего пика, а не II фазы секреции инсулина, что способствует лучшему контролю постпрандиальной гликемии и также уменьшает гиперинсулинемию, являющуюся ключевым патогенетическим звеном повышения веса, атерогеннных нарушений липидного спектра и атеросклероза при СД2 Фармакологическая форма гликлазида МВ на гидрофильном матриксе обеспечивает постепенное высвобождение активного вещества с максимальной концентрацией препарата в дневное время и постепенным снижением ночью, что соответствует суточному профилю гликемии и является дополнительным фактором снижения риска гипогликемий Гликлазид метаболизируется в печени с образованием 7 неактивных метаболитов. Выведение осуществляется в основном почками, менее 1% выводится в неизмененном виде, активные метаболиты в плазме отсутствуют В исследовании ADVANCE (Action in Diabetes and Vascular Disease: PretarAx and DiamicroN Modified Release Controlled Evaluation) [6], где в качестве базовой терапии в группе интенсивного контроля использовался Диабетон МВ, отмечался наименьший риск гипогликемий по сравнению с другими исследованиями по оценке интенсивного контроля гликемии [8, 9], несмотря на то, что 70% пациентов получали препарат в максимальной терапевтической дозе 120 мг/сутки. Наряду с достоверным снижением риска микрососудистых осложнений (нефропатии), ADVANCE показало важную в клиническом отношении тенденцию снижения сердечно-сосудистой смертности на 12 % и общей смертности на 7%. Это исследование убедительно доказало, что выбор наиболее безопасных режимов терапии с меньшим риском гипогликемий имеет определяющее значение для предупреждения сердечно-сосудистых рисков при СД2.
DIAMOND (DIAMicrON MB in Daily practice) – наблюдательная программа по оценке эффективности и безопасности терапии Диабетоном МВ, которая стала попыткой воспроизведения дизайна исследования ADVANCE в условиях повседневной клинической практики.
Основной целью программы было: изучить эффективность терапии Диабетоном МВ в монотерапии и/или комбинации у пациентов с ранее неудовлетворительным контролем СД, а также безопасность стратегии увеличения дозы Диабетона МВ до максимальной (120 мг/сутки).
Дизайн исследования. Многоцентровая нерандомизированная программа с открытым дизайном. Следует подчеркнуть, что исследование предусматривало максимально простой дизайн в условиях реальной клинической практики: последовательное включение пациентов без процедуры рандомизации, отсутствие контрольной группы и минимум обследования. Программа носила только наблюдательный характер и не предусматривала жесткого следования определенным условиям протокола и четких критериев для титрования дозы препарата исследования или добавления и титрования сопутствующей терапии (в случае комбинации). При титровании дозы препарата и назначении комбинированной терапии врачи руководствовались существующими стандартами ведения пациентов с СД2 и личным опытом и знаниями. Период наблюдения – 6 месяцев, количество визитов – 6. На первом визите осуществлялся перевод пациентов на терапию Диабетоном МВ (в монотерапии или комбинации по усмотрению исследователя), на 3 последующих – возможное титрование дозы препарата в зависимости от показателей гликемии, на 5-м визите – оценка эффективности терапии. Дизайн исследования представлен на рисунке 1.
Рис. 1. Дизайн наблюдательной программы DIAMOND
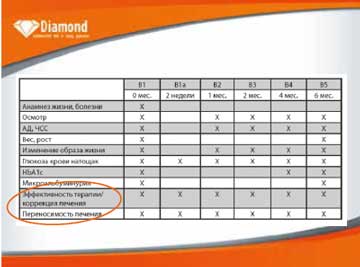
Материалы и методы
В программе участвовало 12 эндокринологических центров Москвы, Московской области, Санкт-Петербурга, Архангельска, Казани, Ростова-на-Дону, Екатеринбурга, Твери, Белгорода, Волгограда, Красноярска, Новосибирска.
В исследование включались пациенты с неудовлетворительным контролем СД2 на терапии диетой или одним ПССП: метформином, глитазоном, ингибитором ДПП-4, акарбозой, глинидом или препаратами СМ (кроме Диабетона МВ).
Все пациенты подписали информированное согласие.
Критерии включения
- Пациенты с СД2 в возрасте старше 35 лет с любой длительностью СД.
- 7,0% < HbA1c < 10,0% на предшествующей терапии диетой или одним ПССП.
Перевод на терапию Диабетоном МВ
В зависимости от наличия и вида предшествующей терапии все пациенты на этапе включения были распределены на две группы.
- На монотерапии диетой (группа А) – препарат назначался в начальной дозе 30 мг/сутки при исходном уровне HbA1c<8,5% или 60 мг/сутки – при HbA1c>8,5%.
- На терапии ПССП (группа В). Если пациент получал не секретагог – допускалась комбинация с ранее принимаемым препаратом или отмена предшествующей терапии и перевод на Диабетон МВ в дозе 30 или 60 мг соответственно уровню HbA1c. Если пациент получал секретагог – предшествующая терапия отменялась и назначался Диабетон МВ в эквивалентной ранее принимаемому препарату дозе (например, 2 таблетки манинила 3,5 мг = 2 таблетки Диабетона МВ, амарил 1 мг=30 мг, 2 мг=60 мг Диабетона МВ соответственно и т.д.).
Критерии оценки эффективности терапии
- Уровень HbA1c через 4 и 6 месяцев терапии.
- Уровень гликемии натощак (ГН) в течение всего периода наблюдения.
- Количество пациентов, достигших уровня HbA1c<7,0% и <6,5% через 4 и 6 месяцев терапии.
- Уровень и динамика альбуминурии (АУ) через 6 месяцев терапии.
- Динамика массы тела.
Критерии оценки безопасности терапии: количество пациентов, у которых отмечались нежелательные явления, в том числе гипогликемии. Оценка переносимости терапии врачом.
Гипогликемией считался уровень глюкозы крови (ГК) <3,9 ммоль/л и/или наличие клинических симптомов, которые расценивались пациентом как типичные проявления гипогликемии, даже в отсутствие подтверждения данными измерения ГК. Гипогликемия расценивалась как легкая, если эпизод самостоятельно купировался пациентом. Тяжелая гипогликемия – эпизод с потерей сознания или без, потребовавший для купирования помощи других лиц.
Критерии оценки наличия осложнений: программа не предусматривала включения в протокол методов оценки наличия осложнений, кроме уровня АУ при включении и через 6 месяцев терапии. Наличие осложнений (ретинопатии, нейропатии, нефропатии) и сопутствующей патологии фиксировалось врачом на основании доступной в медицинских картах информации.
Клиническая характеристика пациентов
В программу было включено 394 пациента с СД2, средний возраст составил 59,0±9,2 лет, средний уровень HbA1c при включении – 8,4±0,9%, ГН – 9,0±1,9 ммоль/л. Клиническая характеристика пациентов при включении представлена в табл. 2.
Таблица 2. Клиническая характеристика пациентов при включении (N=394)
Параметры Среднее значение ± SD, % Возраст, лет 59,0±9,2 Пол, мужской/женский 28,9/71,1 Длительность СД, лет 2,6±3,3 НbA1с, % 8,4±0,9 Гликемия натощак (ГН), ммоль/л 9,0±1,9 Вес, кг 85,4±14,5 Индекс массы тела (ИМТ), кг/м2 31,3±5,1 Систолическое АД (САД), мм рт. ст. 142,1±18,8 Диастолическое АД (ДАД), мм рт. ст. 85,9±10,7 Артериальная гипертония (АГ), % 79,7 Дислипидемия, % 44,4 Диабетическая нефропатия (ДН), % 10,41 Диабетическая ретинопатия (ДР), % 17,51 Диабетическая полинейропатия (ДПН), % 30,96 Заболевания периферических артерий нижних конечностей (ЗПА), % 4,06 Ишемическая болезнь сердца (ИБС), % 20,05 Хроническая сердечная недостаточность (ХСН), % 6,35 Постинфарктный кардиосклероз (ПИКС), % 3,05 Нарушения ритма, % 2,79 Острое нарушение мозгового кровообращения (ОНМК) в анамнезе, % 0,76 HbA1c при оценке компенсации углеводного обмена при включении HbA1c<8,0% имели 35,28% пациентов (n=139), 8,0%≤HbA1c<9,0% – 42,13% пациентов (n=166), 9,0%≤HbA1c<10,0% – 19,04% пациентов (n=75) и HbA1c≥10,0% – 3,55% (n=14). Следует отметить, что в соответствии с критериями включения исходный уровень HbA1c должен быть 7,0% < HbA1c < 10,0%. Тем не менее, у 14 пациентов (3,55%) исходное значение HbA1c было ≥10,0% и у 3 пациентов было равно 7%.
Возраст. Анализ распределения по возрасту показал, что большинство пациентов относились к средней и старшей возрастной группе: 50–59 лет – 42,64% (n=168), 60–69 лет – 28,68% (n=113), 70–79 лет – 14,21% (n=56) пациентов. Другие возрастные группы составили: 40–49 лет – 11,68% (n=46), менее 40 лет – 2,03% (n=8) и более 80 лет – 0,76% (n=3) пациентов соответственно.
Длительность СД: при средней длительности СД2,6±3,3 лет, большинство пациентов имели небольшую продолжительность заболевания: до 1 года – 43,15% (n=170) пациентов, 1–5 лет – 40,36% (n=159), 5–10 лет – 11,68% (n=46), более 10 лет – 3,81% (n=4) и у 1,02% пациентов (n=4) не было данных по этому параметру.
ИМТ: по ИМТ пациенты распределились следующим образом: нормальную массу тела имели лишь 8,88% (35) пациентов, у большинства пациентов исследуемой когорты отмечалась избыточная масса тела (25 < ИМТ < 30 кг/м2) или ожирение I степени (30 < ИМТ < 35 кг/м2): 31,47% (124) и 39,34% (155) пациентов соответственно, ожирение II и III степени –15,48% (61) и 4,83% (19) пациентов соответственно.
Осложнения: у значительной части пациентов отмечались микрососудистые осложнения: у 10,41% – диабетическая нефропатия (ДН), у 17,51% – диабетическая ретинопатия (ДР), у 30,96% – диабетическая полинейропатия (ДПН). Поражение крупных артерий: у 20,05% ишемическая болезнь сердца (ИБС), у 4,06% – заболевания периферических артерий нижних конечностей (ЗПА), 3,05% в анамнезе перенесли инфаркт миокарда (ИМ), 0,76% – острое нарушение мозгового кровообращения (ОНМК). У 79,70% пациентов зафиксирована артериальная гипертония (АГ), у 44,42% – дислипидемия.
Сопутствующая терапия: помимо сахароснижающей терапии, 58,88% пациентов принимали ингибиторы ангиотензинпревращающего фермента (иАПФ), 30,50% – диуретики, 24,37% – бета-блокаторы, 10,41% – блокаторы кальциевых каналов, 7,61% – блокаторы рецептора ангиотензина-II (БРА), 20,05% – статины и 17,01% – антиагреганты. Тем не менее, исходно при включении лишь 6,85% пациентов имели целевой уровень АД (САД<130 и ДАД<80 мм рт. ст.).
Группы пациентов в зависимости от предшествующей терапии
В зависимости от предшествующей терапии пациенты распределились следующим образом: группа А на монотерапии диетой – 28,93% пациентов, группа В1 на предшествующей терапии не секретагогами – 52,03% и группа В2 на терапии секретагогами – 19,54% пациентов.
В таблице 3 представлен перечень препаратов, которые заменялись на Диабетон МВ на первом визите. Из данной таблицы становятся очевидными ряд отклонений от протокола: 1) 10 пациентов получали при включении комбинированный препарат Глибомет, что не соответствует критериям включения – допускалась предшествующая терапия только одним ПССП; 2) согласно табл. 3, препараты СМ (включая пациентов на глибомете) и глиниды были отменены при включении у 70 пациентов (17,77%), в то время как врачами к группе В2 на терапии секретагогами отнесены 77 человек (19,54%), таким образом между заявленной и фактической группой имеется разница в 1,77% или недоучет данных исходной терапии.
Таблица 3. Отмена сахароснижающих препаратов на визите 1
n % Глибенкламид (Манинил) 40 10,15 Глибомет (глибенкламид+метформин) 10 2,54 Репаглинид (Новонорм) 9 2,28 Гликвидон (Глюренорм) 8 2,03 Глимеперид (Амарил) 3 0,76 Акарбоза (Глюкобай) 1 0,25 Всего 71 18,02 Сахароснижающая терапия в ходе исследования Диабетон МВ
На визите включения Диабетон МВ был назначен в дозе 30 мг 70,05% пациентов, в дозе 60 мг – 22,08% пациентов, в дозе 90 мг – 6,35% пациентов, в дозе 120 мг – 1,52% пациентов.
В течение периода наблюдения количество пациентов, получавших Диабетон МВ в дозе 30 мг, сокращалось за счет увеличения количества пациентов, получавших препарат в более высоких дозах. Так, на визите 5 Диабетон МВ в дозе 30 мг получали 22,02% пациентов, в дозе 60 мг – 26,68% пациентов, в дозе 90 мг – 24,09% пациентов, в дозе 120 мг – 27,20% (рис. 2.)
Рис. 2. Доза Диабетона МВ на визите 1 (при включении) по сравнению с визитом 5 (через 6 месяцев терапии)
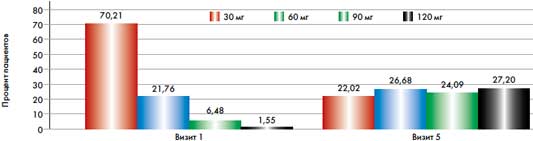
Средняя суточная доза Диабетона МВ увеличилась за 6 месяцев лечения с 41,8 мг на визите 1 до 76,9 мг на визите 5.
Метформин. До включения в исследование метформин принимали 50% пациентов, на первом визите комбинированная терапия Диабетоном МВ и метформином была назначена 57,87% пациентов.
В ходе исследования отмечалось увеличение как количества пациентов, получавших метформин: с 57,87% при включении до 67,26% через 6 месяцев терапии, так и средней суточной дозы метформина: с 1621 мг/сутки до 1685 мг/сутки соответственно. Увеличение средней суточной дозы метформина было статистически значимо, р<0,00001. Увеличение дозы метформина отмечалось у 32,67% пациентов при дозе Диабетона МВ 120 мг, у 21,28% пациентов – при дозе 90 мг, у 20,39% пациентов – при дозе 60 мг и у 11,11% пациентов, получавших 30 мг Диабетона МВ.
Другие ПССП: количество пациентов, получавших в течение наблюдения комбинированную терапию Диабетоном МВ с другими ПССП (не метформином), было ничтожно мало.
Так, акарбозу на визитах 1 и 5 принимали 3 и 1 пациента (0,76–0,25% случаев) соответственно, глитазоны – 4 и 3 пациента (1,02–0,76% случаев), и ДПП-4 – 3 и 5 пациентов (0,76–1,27% случаев), соответственно, 1 пациенту (0,25% случаев) на В5 был добавлен агонист ГПП-1.
Комбинация с инсулином: терапия базальным инсулином была добавлена 2 пациентам (0,51% случаев). Одному пациенту на визите В3 инсулин назначен в дополнение к монотерапии Диабетоном МВ, другому пациенту – на визите В4 в дополнение к комбинации Диабетона МВ и метформина.
Результаты исследования
Оценка эффективности терапии: результаты по различным критериям эффективности суммированы в табл. 4.
Таблица 4. Результаты исследования по различным критериям эффективности
Параметры При включении Через 6 месяцев терапии Изменения за время терапии Р НbA1с, % 8,4±0,9 6,7±0,7 1,6±0,9 P<0,000001 Гликемия натощак, ммоль/л 9,1±1,8 6,0±0,7 3,0±1,8 P<0,000001 Уровень альбуминурии, мг/сутки 59±115 43±92 16,6±49,1 P<0,000001 САД, мм рт. ст. 142,6±17,4 131,6±10,9 10,9±15,3 P<0,000001 ДАД, мм рт. ст. 86,1±9,8 81,2±6,7 4,9±9,9 P<0,000001 ЧСС, в минуту 76,9±8,7 74,5±6,5 2,4±7,9 P<0,000001 Масса тела, кг 85,4±14,5 83,5±13,5 1,9±4,0 P<0,000001
р – различия между уровнем при включении и через 6 месяцев терапии.Через 6 месяцев терапии отмечалось статистически значимое снижение среднего уровня ГН – с 9,1±1,8 ммоль/л при включении до 6,0±0,7 ммоль/л, среднего уровня HbA1c – с 8,4±0,9% до 6,7±0,7% соответственно. Уровня HbA1c<7% достигли 45,43% и 64,72% пациентов через 4 и 6 месяцев терапии, HbA1c<6,5% – 19,03% и 30,71% пациентов соответственно.
Также наблюдались статистически значимые изменения следующих параметров: снижение массы тела, уровня САД и ДАД (табл. 4). При этом количество пациентов с целевыми показателями АД (<130/80 мм рт. ст.) возросло с 6,99% до 11,40%.
В 42,89% случаев врачи оценили эффективность терапии как отличную, в 35,79% как очень хорошую, в 16,24% как хорошую. Неудовлетворительная эффективность терапии, по мнению врачей, отмечена всего в 2,79% случаев. 96,70% пациентов выразили желание продолжить терапию Диабетоном МВ и после завершения программы.
Уровень АУ статистически значимо снизился с 59±115 мг/сут при включении до 43±92 мг/сут через 6 месяцев терапии. Количество пациентов с микроальбуминурией (МАУ) за это время уменьшилось с 29,19% до 22,59%, с протеинурией (ПУ) с 5,08% до 3,30%, и напротив, количество пациентов с нормоальбуминурией (НАУ) возросло до 72,08% (табл. 5).
Таблица 5. Количество пациентов с НАУ, МАУ и ПУ при включении и через 6 месяцев терапии
Норма Микроальбуминурия Протеинурия n % n % n % Визит В1 251 63,71 115 29,19 20 5,08 Визит В5 284 72,08 89 22,59 13 3,30 Следует отметить, что при характеристике осложнений СД при включении врачи отметили наличие ДН всего у 10,41% пациентов, в то время как фактическая частота этого осложнения при проведении исследования на МАУ составила 34,27%, т.е. более чем на 20% выше заявленной, из них у 5% пациентов – на выраженной стадии ПУ. Это является очередным подтверждением того факта, что в реальной клинической практике не уделяется должного внимания диагностике ДН.
Оценка безопасности терапии
В программу были включены 394 пациента, из них 97,97% (386 пациентов) завершили исследование полностью и 2,03% (8 пациентов) выбыли преждевременно, из них в связи с недостаточной эффективностью – 4 пациента (1%). Причины преждевременного выбывания указаны в табл. 6.
Таблица 6. Причины преждевременного исключения
n % Недостаточная эффективность 4 1,02 Отказ пациента 2 0,51 Потеря связи с больным 1 0,25 Состояние не требует применения Диабетона МВ 1 0,25 В 46,95% случаев врачи оценили безопасность терапии как отличную, в 34,01% как очень хорошую, в 16,75% как хорошую, неудовлетворительной оценки безопасности терапии не было ни в одном случае. Выразили желание продолжать терапию Диабетоном МВ и после завершения программы 96,70% пациентов.
Нежелательные явления: нежелательные явления развились у 11 пациентов: из них гипогликемии – у 9 пациентов (2,28%), тошнота – у 1 пациента (0,25%), ОРВИ с последующим обострением хронического бронхита – у 1 пациента (0,25%). Серьезных нежелательных явлений отмечено не было.
Гипогликемии: за период наблюдения зафиксировано 15 случаев гипогликемии у 9 пациентов, что составило 2,28% исследуемой когорты (табл. 7). Случаев тяжелой гипогликемии за весь период наблюдения зафиксировано не было.
Таблица 7. Все случаи гипогликемии в ходе терапии
n % 1 случай гипогликемии 6 1,52 2 случая гипогликемии 1 0,25 3 случая гипогликемии 1 0,25 4 случая гипогликемии 1 0,25 Всего 9 2,28 Обсуждение результатов
Результаты программы DIAMOND показали, что назначение Диабетона МВ в монотерапии или комбинации у пациентов с неудовлетворительным контролем гликемии на предшествующей терапии диетой или одним ПССП обладает выраженным сахароснижающим эффектом и позволяет добиться целевых показателей контроля углеводного обмена у значительной части пациентов: HbA1c<7% через 6 месяцев терапии у 95,43% пациентов, наряду с высоким профилем безопасности терапии: полным отсутствием серьезных нежелательных явлений, низкой частотой гипогликемий (2,28% пациентов) и снижением массы тела.
Следует подчеркнуть, что данные результаты были получены в наблюдательной программе в условиях реальной клинической практики, т.е. в отсутствие жесткого протокола и идеальных условий с привлечением больших материальных и трудозатрат, характерных для крупных рандомизированных исследований.
Большинство пациентов (70%) получали препарат в комбинированной терапии: с метформином – от 58% до 67% пациентов в течение периода наблюдения, с другими ПССП (акарбозой, глитазоном, иДПП-4, агонистом ГПП-1) – 3% пациентов, с инсулином – 0,5% пациентов.
Значительное использование комбинированной терапии, а также статистически значимое увеличение средней суточной дозы метформина в ходе исследования, безусловно, могли повлиять на эффективность лечения и полученные результаты. С другой стороны, большая часть пациентов на комбинированной терапии (группа В1 – 52%) исходно уже получали метформин или другие не секретагоги и тем не менее имели неудовлетворительный контроль СД. При титровании дозы препарата и добавлении комбинированной терапии врачи руководствовались преимущественно собственным опытом и знаниями, поскольку четких критериев титрования протоколом программы предусмотрено не было. Тот факт, что увеличение дозы метформина отмечалось у пациентов, получавших небольшую дозу Диабетона МВ (у 11,11% и 20,39% пациентов при дозе 30 мг и 60 мг соответственно), свидетельствует о том, что резервы титрования дозы основного препарата исследования использовались не в полной мере.
Высокая частота комбинации с метформином, возможно, могла послужить и одним из факторов снижения массы тела: в среднем -1,9 кг (с 85,4±14,5 до 83,5±13,5), что оказалось статистически значимо. Тем не менее, вопреки традиционно сложившемуся мнению о повышении веса на терапии любыми препаратами СМ, многие исследования показали отсутствие значимой динамики массы тела в группах Диабетона МВ: +0,5 кг за 27 недель монотерапии [3], +0,36 кг за 2 года в монотерапии или комбинации с одним ПССП [7], +0,1 кг в течение 5 лет в ADVANCE при комбинированной терапии [10]. В исследовании ADVANCE при анализе показателей в подгруппах оказалось, что повышение веса наблюдалось у пациентов, получавших помимо гликлазида глитазоны и инсулин или их комбинацию, а у пациентов без данной терапии вес снижался как в группе интенсивного, так и стандартного контроля, в среднем на 2 кг [10].
По своим характеристикам пациенты в программе DIAMOND представляли типичную когорту пациентов с СД2: с избыточной массой тела или ожирением (у 92%), сопутствующей АГ (у 80%), дислипидемией (у 44%) и сердечно-сосудистой патологией (ИБС – 20%, атеросклерозом периферических артерий – 4%, ИМ – 3% и ОНМК – 1% в анамнезе). Непрямые эффекты терапии по снижению массы тела и уровня АД, полученные в данном исследовании, следует рассматривать как крайне благоприятные в отношении потенциального снижения сердечно-сосудистого риска у данной категории пациентов.
Безопасность сахароснижающей терапии при СД2 имеет приоритетное значение в силу очень многих причин (пожилого возраста пациентов, сопутствующей сердечно-сосудистой патологии, снижения функции почек, более частых ментальных и когнитивных нарушений).
За 6 месяцев исследования было зафиксировано 15 эпизодов гипогликемии у 9 пациентов, что составило 2,28% исследуемой когорты, тяжелых гипогликемий отмечено не было.
Низкая частота гипогликемий в исследовании отмечалась при значимом снижении уровня HbA1c на 1,6% и достижении HbA1c <7% и <6,5% у 65% и 31% пациентов соответственно. Средняя суточная доза Диабетона МВ составила 76,9 мг/сутки, количество пациентов, получавших препарат в дозе 90 и 120 мг/сутки, – 52%. Для характеристики эпизодов гипогликемии было бы желательно иметь более подробную информацию. В частности важно знать, дневная или ночная гипогликемия, симптоматическая или бессимптомная. Однако эта информация структурой карты в данном исследовании не была предусмотрена. Также не проводился анализ частоты гипогликемий в зависимости от дозы Диабетона МВ. Полученные данные по безопасности терапии Диабетоном МВ, в том числе на терапии в суб- и максимальной дозах, согласуются с данными литературы.
Высокая эффективность Диабетона МВ в достижении целевых показателей углеводного обмена в сочетании с низким риском гипогликемий доказана во многих клинических исследованиях, в том числе в длительном 2-летнем наблюдении [7]. В течение первых 10 месяцев пациенты получали Диабетон МВ или обычную форму препарата, а затем переводились на Диабетон МВ в монотерапии или комбинации с одним ПССП. По окончании наблюдения 53% пациентов получали препарат в максимальной дозе 120 мг, 49% достигли HbA1c≤7%. Во всех группах (на монотерапии и в комбинации), наряду с достоверным по сравнению с исходным уровнем и, что особенно важно, устойчивым в течение 2 лет терапии снижением уровня HbA1c, отмечалась очень низкая частота гипогликемий (4,8 эпизодов/100 пациентов/лет), в том числе в группах риска – у пациентов с начальным и умеренным снижением функции почек и в возрасте старше 65 лет.
В ряде исследований установлены преимущества в отношении безопасности терапии Диабетоном МВ по сравнению с другими препаратами СМ – глимепиридом [3] и глибенкламидом [4, 5]. Так, в исследовании GUIDE (GlUcose control in tipe 2 diabetes: Diamicron MR vs. glimEpiride) [3] при равном сахароснижающем эффекте препаратов и одинаковом количестве пациентов, достигших целевого уровня HbA1c<7% (50% в обеих группах), терапия Диабетоном МВ ассоциировалась с 50% снижением риска развития гипогликемий по сравнению с глимепиридом: количество эпизодов с уровнем гликемии <3 ммоль/л составило 3,7% против 8,9%, р=0,003, с уровнем гликемии от 3 до 4 ммоль/л – 7,7% против 14,4%, р=0,002. Кроме того, отмечались выраженные различия в частоте гипогликемий у пациентов с уровнем HbA1c≤6,5%: 2,1% против 17,5% и у пациентов с умеренным снижением функции почек (клиренс 50–80 мл/мин): 3,2% против 12,6%, р<0,02.
В исследовании ADVANCE Диабетон МВ использовался в качестве базового препарата в группе интенсивной терапии, более 70% пациентов по окончании 5-летнего периода наблюдения получали максимальную дозу 120 мг. В ADVANCE отмечался наименьший риск гипогликемий по сравнению с аналоговыми исследованиями по оценке интенсивного лечения СД2, при этом большинство пациентов в группе интенсивной терапии достигли очень жестких критериев контроля HbA1c: ≤7% – 80%; (6,0–6,5)% – 43,6% и ≤6,0% – 21,3% пациентов [10]. ADVANCE убедительно продемонстрировало, что тактика постепенного достижения целевого контроля гликемии посредством поэтапной интенсификации терапии является оптимальной по соотношению эффективность/безопасность. Это исследование оказалось самым успешным как в отношении безопасности терапии [11], так и микрососудистых и сердечно-сосудистых исходов [12] по сравнению с ACCORD [8] и VADT [9], где стратегия агрессивной многокомпонентной терапии, приведшей к достоверному повышению частоты тяжелых гипогликемий в группах интенсивного контроля, явилась одним из основных факторов повышения смертности.
Таким образом, Диабетон МВ доказал высокий профиль безопасности и может рассматриваться в качестве препарата выбора среди производных СМ у пациентов с высоким риском развития гипогликемий, а также для достижения жестких целевых параметров контроля СД2.
Еще один аспект в отношении безопасности терапии препаратами СМ представлется крайне важным – это данные о различном влиянии на сердечно-сосудистую патологию и смертность. Гликлазид, молекула которого не содержит бензамидной группы, имеющей сродство к сердечной мышце и сосудам, проявляет в 16 000 раз большую селективность к SUR1 рецепторам, практически не оказывая влияния на миокард [2]. Селективно взаимодействуя с рецептором β-клеток, гликлазид, в отличие от глибенкламида [13], не нарушает процессы так называемого ишемического прекондиционирования [14], т. е. адаптацию миокарда к ишемии. И хотя однозначное мнение по проблеме сердечно-сосудистой безопасности различных представителей класса см не сформировано, в ряде популяционных исследований и ретроспективных анализов терапия глибенкламидом ассоциируется с достоверным повышением риска ИБС и ИМ [15, 16], а также общей [17–20] и сердечно-сосудистой смертности [19, 20], в отличие от гликлазида и глимепирида, с наименьшими показателями риска на терапии гликлазидом [20]. Кроме того, уникальные гемореологические и антиоксидантные свойства, не связанные с сахароснижающим действием (снижение агрегации тромбоцитов, восстановление баланса простациклина и тромбоксана А2, усиление фибринолиза, угнетение оксидативного стресса за счет стимуляции активности супероксиддисмутазы) [21] могут быть дополнительным аргументом в пользу оптимальной переносимости и выбора препарата у пациентов с СД2 с сердечно-сосудистой патологией.
Одним из важнейших результатов DIАMOND стало достоверное снижение уровня АУ, а также количества пациентов с МАУ и ПУ, несмотря на очень небольшую продолжительность исследования. Безусловно, просто констатировать факт положительной динамики АУ на фоне терапии сахароснижающим препаратом было бы некорректно. Так, дизайн исследования не позволяет оценить динамику этого показателя в зависимости от нефропротективной терапии, например, ингибиторов АПФ. Следует отметить, что обратной стороной относительно «щадящего дизайна» в любой наблюдательной программе является несколько меньшее «качество» данных по сравнению с рандомизированными клиническими исследованиями. В частности, когорта пациентов в наблюдательных программах может быть весьма неоднородна из-за отсутствия процедуры рандомизации. Данное исследование не стало исключением, на что указывает непараметрическое распределение таких показателей, как величина АУ исходно и через 6 месяцев терапии (табл. 5). Тем не менее, в программе DIAMOND удалось подтвердить эффективность, безопасность и органопротективные свойства контроля гликемии на терапии Диабетоном МВ, полученные в крупном рандомизированном контролируемом исследовании ADVANCE. Результаты ADVANCE, показавшие достоверное снижение частоты целого спектра почечных исходов, в том числе развития или прогрессирования ДН на 21%, новых случаев МАУ на 9%, ПУ на 30% [6], доказали определяющее значение контроля гликемии в снижении риска микрососудистых осложнений. Регресс ДН как минимум на одну стадию был выявлен у 62% пациентов, большинство из которых достигли НАУ. Следует особо подчеркнуть, что протективный эффект интенсивного контроля гликемии в ADVANCE отмечался даже у тех пациентов, которые исходно имели HbA1c<7% [22]. Это еще раз подтверждает, что для снижения риска микрососудистой патологии нижнего предела HbA1c может не существовать, и оптимальным является максимальное приближение к нормогликемии.
Заключение
Программа DIАMOND показала, что терапия Диабетоном МВ позволяет эффективно достигать целевых параметров контроля СД без увеличения риска гипогликемий и повышения массы тела на фоне улучшения контроля гликемии, несмотря на непродолжительный период наблюдения, отмечались не-фропротективные эффекты (снижение уровня альбуминурии и регресс МАУ до нормоальбуминурии у 7% пациентов). Результаты программы в очередной раз продемонстрировали сообществу практикующих врачей, что основной целью терапии СД2 является целевой контроль гликемии, а также реальные возможности современных препаратов СМ в достижении этой цели.
ЛИТЕРАТУРА
1. Шестакова М.В. Из доклада «Новые рекомендации по терапии СД2 в России». Обучающий курс Joslin Diabetes Center и ЭНЦ МЗРФ. – М., 25 мая 2011 г.
2. Gribble F.M., Reimann F. Differential selectivity of insulin secretagogues: mechanisms, clinical implications, and drug interactions // J. Diabetes Complications. – 2003. – № 17. – Р. 11–15.
3. Schernthaner G., Grimaldi A., Di Mario U., Drzewoski J., Kem-pler P., Kvapil M., Novials A., Rottiers R., Rutten G. E. H. M. and Shaw K. M. GUIDE study: double-blind comparison of once-daily gliclazide MR and glimepiride in type 2 diabetic patients // European Journal of Clinical Investigation. – 2004. – № 34. – Р. 535–542.
4. Tessier D., Dawson K., Tetrault J.P., Bravo G., Meneilly G.S. Gliben-clamide vs gliclazide in type 2 diabetes of the elderly // Diabet Med. – 1994. – № 11. – Р. 974–980.
5. Veitch P.C., Clifton-Bligh R.J. Long-acting sulfonylureas – long-acting gy-poglycaemia // Med. J. Aust. – 2004. – № 180. – Р. 84–85.
6. Patel A., MacMahon S., Chalmers J., Neal B. et al. The ADVANCE Collaborative GrouP. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes // N. Engl. J. Med. – 2008. – № 358. – Р. 2560–2572.
7. Drouin1 P., Standl E. for the Diamicron MR Study GrouP. Gliclazide modified release*: results of a 2-year study in patients with type 2 diabetes // Diabetes, Obesity and Metabolism. – 2004. – № 6. – Р. 414–421.
8. Gerstein H.C., Miller M.E., Byington R.P., Goff D.C. et al. The Action to Control Cardiovascular Risk in Diabetes Study Group: effects of intensive glucose lowering in type 2 diabetes // N. Engl. J. Med. – 2008. – № 358. – Р. 2545–2559.
9. Duckworth W., Abraira C., Mortiz T., Reda D. et al. VADT Investigators. Glucose control and vascular complications in veterans with type 2 diabetes // N. Engl. J. Med. – 2009. – № 360. – Р. 129–139.
10. Zoungas S., Chalmers J., Kengne A.P., Pillai A., Billot L., de Galan B., Marre M., Neal B., Harrap S., Poulter N., Patel A. The efficacy of lowering glycated haemoglobin with a gliclazide modified release-based intensive glucose lowering regimen in the ADVANCE trial // Diab. Res. Clin. Pract. – 2010. – № 89. – Р. 126–133. doi:10.1016/j.di-abres.2010.05.012.
11. Desouza C.V., Bolli G.B., Fonseca V. Hypoglycemia, diabetes, and cardiovascular events // Diabetes Care. – 2010. – № 33(6). – Р. 1389–1394.
12. Skyler J.S., Bergenstal R., Bonow R.O., Buse J. et al. Intensive glycaemic control and the prevention of cardiovascular events: implications of the ACCORD, ADVANCE, and VA Diabetes Tials: A Position Statement of the American Diabetes Association and a Scientific Statement of the American College of Cardiology Foundation and the American Heart Association // Circulation. – 2009. – № 119. – Р. 351–357.
13. Klepzig H., Kober G., Matter C. et al. Sulfonylureas and ischemic preconditioning: a double-blind, placebo-controlled evaluation of glimepiride and glibenclamide // Eur. Heart J. – 1999. – № 20. – Р. 439–446.
14. Maddock H.L., Siedlecka S.M., Yellon D.M. Myocardial protection from either ischemic preconditioning or nicorandil is not blocked by glicla-zide // Cardiovasc Drugs Ther. – 2004. – № 18. – Р. 113–119.
15. Thisted H., Johnsen S.P., Rungby J. Sulfonylureas and the risk of myocar-dial infarction // Metabolism. – 2006. – № 55. – S16–S19.
16. Johnsen S.P., Monster T.B., Olsen M.L. et al. Risk and short-term prognosis of myocardial infarction among users of antidibetic drugs // Am. J. Ther. – 2006. – № 13. – Р. 134–140.
17. Monami M., Balzi D., Lamanna C., Barchielli et al. Are sulfonylureas all the same? A cohort study on cardiovascular and cancer related mortality // Diabetes Metab. Res. Rev. – 2007. – № 23. – Р. 479–484.
18. Monami M., Luzzzi C., Lamanna C. et al. Three-year mortality in diabetic patients treated with different combinations of insulin secretagogues and metformin // Diabetes Metab. Res. Rev. – 2006. – № 22. – Р. 477–482.
19. Khalangot M., Tronko M., Kravchenko V., Kovtun V. Glibenclamide-related excess in total and ardiovascular mortality risks: data from large Ukrainian observational cohort study // Diabetes Res. Clin. Pract. – 2009. – № 86. – Р. 247–253.
20. Schramm T.K., Gislason G.H., Vaag A., Rasmussen J.N. et al. Mortality and cardiovascular risk associated with different insulin secretagogues compared with metformin in type 2 diabetes, with or without a previous myocardial infarction: a nationwide study // European Heart Journal. – 2011. – doi:10.1093/eurheartj/ehr077.
21. Gram J., Jespersen J. Increased fibrinolytic potential induced by gli-clazide in types I and II diabetic patients // Am. J. Med. – 1991. – № 90. – P. 62S–66S.
22. Zoungas S., Chalmers J., Patel A., et al. Intensive glucose control is reno-protective in type 2 diabetes: new analyses from ADVANCE. Abstracts of 46th annual meeting of the European Association for the Study of Diabetes, 2010 // Diabetologia. – 2010. – № 53(Suppl1). – S98.Викулова Ольга Константиновна, к.м.н., вед.н.с. отделения диабетической нефропатии и гемодиализа, ФГУ Эндокринологический научный центр, Москва
Шестакова Марина Владимировна, д.м.н., проф., директор Института диабета, ФГУ Эндокринологический научный центр, Москва
| Февраль 2014 г. |