Опубликовано в журнале:
« Психиатрия » №1, стр. 37-50, 2009.Исследование эффективности и безопасности применения актовегина у больных пожилого возраста с синдромом мягкого когнитивного снижения церебрально-сосудистого генеза
Селезнева Н.Д., Михайлова Н.М., Калын Я.Б., Рощина И.Ф., Гаврилова С.И.
Научный центр психического здоровья РАМН, МоскваИзучалась эффективность препарата Актовегин в лечении синдрома мягкого когнитивного снижения (Mild cognitive impairment — MCI) церебрально-сосудистого генеза. 30 пациентов (7 мужчин и 23 женщины; средний возраст 71,2 года) получали Актовегин внутримышечно по 5 мл (200 мг) ежедневно в течение 4 недель. Для формализованной оценки состояния пациентов до и после лечения использованы шкала общего клинического впечатления (CGI), мини-тест для оценки когнитивного статуса (MMSE), тест «Вербальные ассоциации», шкала лобной дисфункции, тест рисования часов, Бостонский тест называния, тест деменции Маттиса, тест запоминания 10 слов, шкала депрессии Гамильтона. Достоверное улучшение достигнуто по показателям всех оценок. Установлен позитивный терапевтический эффект: увеличение скорости психических процессов, уменьшение выраженности брадипсихизма и дисмнестических расстройств, а также положительное влияние на астенические и депрессивные симптомы. Побочных эффектов и нежелательных явлений на терапии Актовегином не наблюдалось. Сделан вывод о показаниях к широкому применению препарата у пожилых пациентов с начальными проявлениями когнитивного снижения.
Ключевые слова: цереброваскулярная болезнь; MCI; лечение; Актовегин.In this study was investigated effectiveness of Aktovegin drug in treatment of mild cognitive impairment (Mild cognitive impairment — MCI) of cerebro-vascular genesis. 30 patients (7 m and 23 f, average age 71.2 years) received Aktovegin intramuscularly to 5 ml (200 mg) daily during 4 weeks. For formal assessment of patients before and after treatment used by scale of clinical global impression (CGI), mini mental state examination (MMSE), verbal association test, scale of frontal dysfunction, clock drawing test, Boston naming test, Mattis dementia test, test to remember 10 words, Hamilton depression scale. Credible performance improvement achieved by all of estimates. A positive therapeutic effect: increased speed of mental processes, reduced bradipsychism and dismnestic disorders expression, as well as positive impact on asthenic and depressive symptoms. Side effects and adverse events effects on Aktovegin therapy were notobserved. It is concluded that testimony to wide application of drug in elderly patients with early manifestations of cognitive decline.
Key words: cerebrovascular disease, MCI, treatment, Aktovegin.Синдром мягкого когнитивного снижения (MCI)1(1 Синдром MCI в ряде работ отечественных неврологов [3, 4] именуется умеренным когнитивным снижением (УКС)) характеризуется пограничным расстройством памяти и когнитивных функций, степень проявления которых не позволяет поставить диагноз деменции церебрально-сосудистого или иного генеза, в том числе болезни Альцгеймера (БА) [2].
Распространенность синдрома MCI в пожилом возрасте исключительно велика. Среди населения Москвы в возрасте старше 60 лет этот показатель составляет около 18% [5]. Аналогичные цифры (19%) приводят O. Lopez и соавт. [16]. Как было показано отечественными исследователями [9], у 40% лиц с установленным диагнозом MCI в течение 4 лет диагностируется БА или деменция иного генеза.
В последние годы получены доказательства гетерогенности синдрома МСI, в связи с чем выделены различные клинические варианты синдрома (амнестический, неамнестический и вариант с множественной когнитивной недостаточностью), имеющие различный прогноз сточки зрения вероятности перехода в разные нозологические типы деменции (болезнь Альцгеймера, церебрально-сосудистую или лобно-височную деменцию, деменцию с тельцами Леви и др.).
Начальные проявления синдрома МСI с множественной когнитивной недостаточностью чаще всего ассоциированы с высоким риском утяжеления сосудистого заболевания, включая повышенный риск нарушений мозгового кровообращения, а также риск развития деменции даже при безинсультном течении [6; 16].
В связи с этим задачи лечения MCI церебрально-сосудистого генеза у пациентов пожилого и старческого возраста выдвинулись в разряд наиболее актуальных в гериатрической практике и составляют повседневное содержание деятельности как неврологов и психиатров, так и врачей общей практики. Это объясняется прежде всего общеизвестной широкой распространенностью цереброваскулярных заболеваний, в первую очередь церебрального атеросклероза, среди начальных клинических симптомов которого наиболее часто наблюдается легкое когнитивное снижение. Частота хронической ишемии головного мозга (ДЭ) определяется в 70-100 случаев на 1000 населения [9], а нарушение когнитивных функций признается одним из наиболее часто встречающихся проявлений цереброваскулярной болезни. По данным популяционных исследований [1], начальные проявления этого расстройства выявляются у 24,4% городского населения пожилого и старческого возраста (60 лет и старше), а среди пожилых пациентов ПНД — в 18,7%. При сплошном обследовании пожилого контингента пациентов территориальной поликлиники эти нарушения обнаружены в 30,8% [7]. Легкое когнитивное снижение в рамках сосудистого психоорганического синдрома в 24,5% случаев является причиной обращения к геронтопсихиатру общесоматической поликлиники, а еще в 36,2% наблюдений диагностируется как коморбидное расстройство у пациентов геронтопсихиатрического кабинета [7].
Актуальность раннего терапевтического вмешательства при выявлении обусловленных церебрально-сосудистыми заболеваниями легких когнитивных нарушений или синдрома MCI церебрально-сосудистого генеза очевидна, поскольку существует большая социальная и медицинская заинтересованность в эффективном лечении этого синдрома, которое возможно проводить даже в первичном звене здравоохранения [13; 15]. Наряду с рутинной гипотензивной терапией и коррекцией проявлений системного атеросклероза лечение начальных проявлений когнитивного снижения является одной из важнейших задач комплексной терапии, направленной в том числе на профилактику деменции у лиц пожилого возраста.
Существующие в настоящее время методы лечения начального когнитивного снижения MCI церебрально-сосудистого генеза включают следующие основные направления терапевтического вмешательства: улучшение реологических параметров; улучшение доставки и использования кислорода и глюкозы в церебральных структурах; устранение или уменьшение нейротрансмиттерной недостаточности.
Актовегин — высокоочищенный гемо-диализат, получаемый методом ультрафильтрации из крови молодых бычков в возрасте до 6 месяцев. Препарат содержит исключительно физиологические компоненты, обладающие высокой биологической активностью — органические низкомолекулярные соединения: аминокислоты, олигопептиды, нуклеозиды; промежуточные продукты углеводного и жирового обмена: олигосахариды и гликолипиды. Молекулярные массы органических соединений, входящих в состав Актовегина, не превышают 5000 дальтон. Технология получения гемодиализата исключает наличие белковых и других компонентов, обладающих антигенными и пирогенными свойствами. Проведенные экспериментальные и клинические исследования доказали, что Актовегин не содержит дополнительных примесей компонентов крови.
Терапевтическая эффективность Актовегина обусловлена широким спектром входящих в его состав веществ: аминокислот, олигопептидов (инсулиноподобного действия), нуклеозидов, электролитов (калия, натрия, фосфора, магния, кальция, меди) и микроэлементов, а также промежуточных продуктов обмена (олигосахаридов, гликолипидов).
Фармакологическое действие. Актовегин — современный антигипоксант, применяемый для лечения и профилактики гипоксических и ишемических нарушений органов и тканей. Актовегин принадлежит к группе препаратов без прямого вазодилатирующего воздействия. Препарат действует как нейрометаболический стимулятор, увеличивая энергообеспечение нервных клеток путем усиления потребления и утилизации кислорода и глюкозы в нервных клетках, что приводит к улучшению мозговых функций. Многочисленные исследования показали, что Актовегин, улучшая усвоение кислорода и глюкозы нервными клетками, оказывает активизирующее действие на метаболические процессы в головном мозге. В условиях повышения потребления глюкозы соответственно возрастает и потребление кислорода. Эти процессы приводят к ускорению синтеза АТФ в головном мозге, стимуляции всего клеточного метаболизма, улучшению кровоснабжения ишемизированной ткани мозга, что обеспечивает отчетливый терапевтический эффект при нарушениях мозгового кровообращения. Актовегин увеличивает концентрации АТФ, АДФ, а также аминокислот — глутамата, аспартата и ГАМК.
Помимо этого, Актовегин обладает инсулиннезависимым инсулиноподобным действием, за счет которого повышается активность переносчиков глюкозы до 50% максимальной эффективности инсулина. Олигосахариды, входящие в состав Актовегина, имитируюттакие эффекты инсулина как стимуляция липогенеза, ингибирование липолиза, торможение образования внутриклеточного цАМФ и активация транспорта глюкозы в клетку.
Поступление большого количества кислорода вызывает активацию аэробного окисления, что в свою очередь увеличивает энергетический потенциал клетки. Актовегин улучшает энергообмен в эндотелии сосудов, что ведет к высвобождению эндогенных веществ с вазодилатирующими свойствами — простациклина и оксида азота — и улучшению перфузии всех тканей и снижению периферического сопротивления. В условиях тканевой гипоксии, вызванной нарушением микроциркуляции, актовегин способствует восстановлению капиллярной сети за счет новообразующихся сосудов. Улучшая доставку кислорода и уменьшая выраженность ишемических повреждений тканей, Актовегин опосредованно способствует белоксинтезирующей функции клеток.
Антигипоксический эффект Актовегина наиболее выражен в условиях внутриклеточной недостаточности кислорода, в частности вследствие гипоксии или гипоперфузии, причем антигипоксическое действие Актовегина распространяется не только на нейрональные, но и на глиально-клеточные структуры. Показано, кроме того, увеличение кровотока в сером веществе, усиление поступления глюкозы через ГЭБ и внутрь клеток.
Антигипоксическое действие Актовегина начинает проявляться не позднее чем через 30 мин (10-30 мин) после парентерального введения и достигает максимума в среднем через 3 ч (2-6 ч).
В связи с тем, что Актовегин улучшает микроциркуляцию и оказывает активирующее действие на метаболические процессы в головном мозге, представляется обоснованным изучение эффективности его применения у пожилых пациентов с когнитивными нарушениями церебрально-сосудистого генеза. Хотя Актовегин известен около 40 лет в качестве классического нейрометаболического препарата, однако отношение к его применению в качестве к ноотропного средства подвергалось колебаниям от сомнений до доказательных утверждений. В ряде контролируемых исследований была показана эффективность Актовегина при когнитивных расстройствах различной степени тяжести [7; 8; 10; 13; 15; 17; 18; 20], в том числе при деменции сосудистой и альцгеймеровской природы [8; 10; 13]. В большинстве исследований показаны преимущества парентерального введения Актовегина методом внутривенных инфузий по 250 мл (2000 мг) курсом не менее 10 вливаний; при этом указывается на более быстрое наступление воздействия на когнитивные нарушения. Редукция или нивелирование расстройств памяти и внимания, возрастание темпа психических процессов регистрируются более чем у половины пациентов. Отсутствуют данные о результатах другого способа парентерального введения Актовегина — внутримышечного, значительно более удобного для широкого применения в амбулаторной практике.
Цель настоящей работы состояла в изучении эффективности и безопасности внутримышечного применения Актовегина у пациентов пожилого возраста с синдромом мягкого когнитивного снижения церебрально-сосудистого генеза.
Исследование проводилось как открытое неконтролируемое в группе пациентов с синдромом MCI церебрально-сосудистого генеза, находящихся под наблюдением сотрудников отдела по изучению болезни Альцгеймера и ассоциированных с ней расстройств НЦПЗ РАМН.
Критерии включения пациентов в исследование:
1. женщины (в постменопаузальном периоде) и мужчины в возрасте от 50 до 85 лет;
2. оценка по шкале MMSE ≥ 26 баллов;
3. соответствие критериям диагностики синдрома мягкого когнитивного снижения (MCI):а) жалобы больного на легкое снижение памяти, подтверждаемые информантом (обычно членом семьи), и объективно выявляемые признаки легких когнитивных дисфункций;
б) оценка 0,5 по шкале CDR;
в) отсутствие оснований для диагноза деменции;
г) сохранность повседневной активности, хотя может быть легкое ухудшение в сложных и инструментальных видах повседневной и /или профессиональной деятельности;
4. оценка по шкале Хачински > 4;
5. получение письменного информированного согласия от пациента.Критерии исключения:
1. диагноз деменции по критериям DSM-IV, МКБ-10;
2. неврологические заболевания (врожденные и/или приобретенные метаболические энцефалопатии, токсические и лекарственные энцефалопатии, болезнь Паркинсона, инсульт, эпилепсия, инфекционные заболевания, демиелинизирующие и наследственно-дегенеративные заболевания ЦНС);
3. неопластические и /или травматические повреждения головного мозга;
4. системные заболевания;
5. психические заболевания;
6. тяжелая органная патология; злокачественные экстрацеребральные опухоли, ВИЧ-инфекция, сахарный диабет в стадии декомпенсации или другие эндокринные заболевания; алкоголизм и /или лекарственную зависимость; медикаментозная или иная интоксикация;
7. депрессия с оценкой > 18 баллов по шкале Гамильтона для депрессии;
8. уровень систолического давления > 180 мм рт. ст., диастолического > 95 мм рт. ст.;
9. дефицит фолиевой кислоты и /или витамина В12;
10. гипотиреоз.Схема назначения препарата: в конце вводного периода, длящегося до 7 дней, пациентам, отвечающим требованиям включения/исключения в исследование, назначали Актовегин в дозе 200 мг (5 мл) в /м в течение 28 дней. Препарат вводили вне зависимости от приема пищи 1 раз в сутки. Катамнестическое исследование проводилось через 28 ± 5 дней после завершения терапии.
Из сопутствующей терапии допускалось применение короткодействующих бензодиазепиновых препаратов и препаратов, направленных на лечение соматической патологии в том случае, если лечение ими началось за 1 месяц до настоящего исследования и продолжалась на протяжении всего исследования в стабильных дозах.
Оценка состояния пациентов в процессе лечения по шкалам проводилась в фиксированные дни: 0-й день (до начала терапии), 14-й день исследования, 28-й день исследования (окончание лечебного курса), 56-й день (катамнез). Перед началом и в ходе исследования использовались следующие методы обследования больных: объективное клиническое обследование, ЭКГ, лабораторные анализы крови и мочи.
Методы оценки эффективности терапии. В соответствии с рекомендациями S. Kanowski [15], эффективность ноотропного препарата должна оцениваться по трем направлениям: психопатологически (оценка клинических симптомов); психометрически (тестирование); по поведению (самооценка и оценка другими лицами с учетом возрастных особенностей).
Для оценки состояния когнитивных функций и повседневной активности пациентов применялись следующие шкалы и тесты: CDR, шкала Хачински, CGI (шкала общего клинического впечатления), MMSE (короткий тест для оценки когнитивного статуса), тест «Вербальные ассоциации», Шкала лобной дисфункции, Тест рисования часов, Бостонский тест называния, Шкала деменции Маттиса, Тест запоминания 10 слов, шкала депрессии Гамильтона.
Тест «Вербальные ассоциации» предназначен для исследования ассоциативного мышления и заключается в назывании за 1 минуту слов с заданным признаком (начинающихся, например, на букву «к»).
Шкала лобной дисфункции направлена на исследование произвольной регуляции деятельности, связанной с лобными структурами, и включает несколько тестов, характеризующих концептуализацию, звуковые ассоциации, динамический праксис, простую и усложненную реакции выбора. Тест «Звуковые ассоциации» аналогичен тесту «Вербальные ассоциации». Тест «Концептуализация» также заключается в назывании слов на заданный признак (например, называние животных за 1 минуту). С помощью теста «Динамический праксис» оценивается работа заднелобных структур головного мозга. В тестах «Простая и усложненная реакции выбора» определяется произвольная регуляция праксиса, обеспечиваемая передней ассоциативной зоной коры больших полушарий.
Тест рисования часов направлен на диагностику сохранности зрительно-пространственной деятельности. С помощью Бостонского теста называния исследуется номинативная функция речи. Тест представляет собой 55 картинок, изображающих предметы, которые нужно точно назвать.
Шкала деменции Маттиса — это комплексная методика, включающая оценку мнестико-интеллектуальной сферы при деменциях позднего возраста. Методика состоит из нескольких шкал, в том числе на реципрокную координацию, определение сходства, оценку памяти и графомоторную пробу. Шкала «реципрокная координация» — это проба, направленная на исследование динамического праксиса, а также межполушарного взаимодействия. «Графомоторная проба» предназначена для изучения динамического праксиса. Тест «Сходства» позволяет исследовать уровень обобщения. По шкале «Память» оцениваются различные компоненты мнестической функции — зрительная и слухоречевая память.
Тест запоминания 10 слов направлен на изучение способности произвольного запоминания в слухоречевой сфере.
Безопасность препарата оценивалась по Шкале оценки нежелательных явлений.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
В исследование включено 30 больных с синдромом мягкого когнитивного снижения церебрально-сосудистого генеза (7 мужчин, 23 женщины) в возрасте от 53 до 84 лет (в среднем 71,2 ± 8,0 года), находившихся на стационарном или амбулаторном лечении. Возраст начала заболевания в среднем составил 67,8 ± 7,9 года (от 52 до 81 года). Давность заболевания во всех случаях (за исключением одного) совпадала с продолжительностью психопатологического состояния, явившегося показанием к назначению Актовегина, и составляла от 1 года до 7 лет (в среднем 3,3 года). Следует отметить, что у всех пациентов при достаточно большой длительности расстройств, отвечающих критериям синдрома MCI, отсутствовали признаки явного прогрессирования когнитивных нарушений. Во всех случаях оценка по шкале общего снижения (Global Deterioration Scale — GDS) соответствовала пункту 3, что отражает самые начальные проявления заболевания [19]. Оценка когнитивного статуса по Клиническому рейтингу деменции (Clinical Dementia Rating — CDR [Morris J. C., 1993]) также во всех случаях не превышала значения 0,5, что исключало или делало диагностику деменции сомнительной из-за легкой степени расстройств. По МКБ-10 легкое когнитивное расстройство, главным признаком которого является снижение когнитивной продуктивности: нарушение памяти, трудности в обучении, ослабление концентрации внимания, соответствовало рубрике F06.7.
По шкале общего клинического впечатления о тяжести заболевания (Clinical Global Impression — Severity, CGI-S) состояние больных было квалифицировано как пограничное расстройство у 10 пациентов, а в остальных 20 наблюдениях — как «легкое заболевание».
В 3 случаях легкое когнитивное расстройство сочеталось с коморбидной депрессией легкой степени тяжести (14-16 баллов по шкале депрессии Гамильтона — Hamilton Depressive scale, HAMD). Еще у 12 пациентов имелись отдельные депрессивные симптомы (5-13 баллов по HAMD), совокупность которых не отвечала критериям депрессивного синдрома, а их проявления совпадали с соматическими жалобами или перекрывались астеническими симптомами. Среднегрупповой суммарный балл до начала лечения Актовегином по HAMD составил 9,1. В психопатологическом анамнезе наряду с легким когнитивным снижением и псевдоневрастеническими расстройствами у 5 больных выявлены очерченные во времени эпизоды психопатологических расстройств, имевшие место за два-три года до включения в настоящее исследование. Одна больная перенесла в прошлом делирий, у другой больной развилась депрессия после ОНМК, еще у 3 пациентов ранее отмечались психогенные депрессивные реакции.
Выяснение неврологического анамнеза выявило у 9 больных ранее перенесенные острые нарушения мозгового кровообращения — в 5 случаях в видетранзиторных ишемических атак (ТИА), остальные 4 больных переносили ишемические инсульты (в одном из этих случаев — повторно). Оценка по шкале Хачински к началу исследования колебалась в диапазоне от 4 до 10 баллов (в среднем 6 баллов).
Неврологический диагноз всех включенных в исследование пациентов формулировался как ДЭ 1-3-й степени гипертонического, атеросклеротического или смешанного типа [11]. В неврологическом статусе в одном наблюдении отмечены остаточные явления гемипареза и гемигипестезии, у 5 больных — тремор пальцев рук, в остальных случаях неврологические симптомы исчерпывались рассеянной микросимптоматикой и явлениями динамической атаксии.
Ранее проводимое лечение по поводу когнитивных нарушений почти у половины пациентов (14 человек) включало кавинтон, 8 больных в прошлом лечились церебролизином, в отдельных случаях пациенты ранее получали мексидол, препараты Гинкго Билоба, пикамилон, проноран, сермион. Эффективность предшествующего лечения была различной. К началу терапии Актовегином у всех пациентов отмечалась декомпенсация когнитивных и астенических (псевдоневрастенических) расстройств.
Состояние пациентов до начала лечения Актовегином характеризовалось комплексом симптомов различного характера и разной степени выраженности. Общим для всех пациентов было сочетание признаков легкого когнитивного снижения и выраженных в разной степени и объеме астенических (псевдоневрастенических) нарушений.
Причиной обращения за врачебной помощью были в первую очередь жалобы на забывчивость и различные проявления астении. Проявления забывчивости описывались больными как трудности запоминания или припоминания, утрата естественной легкости в подборе слов, «как будто что-то застопорилось». Пациенты жаловались на рассеянность, замедление сообразительности, признавали, что им «непросто собраться с мыслями», вспомнить о недавних намерениях, особенно при отвлечении внимания, но, как отмечали пациенты, они в последующем могли спонтанно припомнить необходимое. Большинство пациентов, за редким исключением, жаловались на частые или постоянные головные боли, иногда только в одной половине головы, но чаще без четкой локализации, либо тяжесть в голове, описывали тягостные ощущения в голове в виде «стягивания обручем» или «давления на глаза, на уши». Помимо этого, многие больные жаловались на постоянный «звон» в ушах, шум, «гул» в голове.
Следующими по частоте были жалобы неустойчивость равновесия, пошатывание при ходьбе или ощущение, что «земля уходит из-под ног». Помимо этого, больные отмечали быстрое наступление усталости после небольших нагрузок, даже после еды, уборки постели, утомление и снижение работоспособности, слабость со стремлением прилечь. Ухудшение общего самочувствия сопровождалось нарушением сна, трудностями засыпания, уменьшением глубины и продолжительности сна, обильными яркими сновидениями, иногда устрашающего содержания или утомительно изменчивого бессмысленного содержания, в отдельных наблюдениях с гипнагогическими зрительными обманами восприятия. Утреннее пробуждение характеризовалось трудностями перехода от сна к бодрствованию, отсутствием ощущения отдыха после сна. Некоторые пациенты жаловались на дневную сонливость, дремоту, мешающую привычной деятельности.
Пациенты замечали появление слезливой обидчивости или обостренной чувствительности к обычным впечатлениям от увиденного или услышанного. Неустойчивость настроения характеризовалась легкостью возникновения реакций раздражения, нетерпения, нередко пациенты отмечали усиление этих проявлений после беспокойной ночи с частыми пробуждениями. Склонность к пессимистической оценке обыденных явлений и жизненных событий могла сочетаться с наплывом безотчетной тревоги и утрированного беспокойства. Содержание тревожных опасений зачастую определяло появление забывчивости, сосредоточенность на заболевании в целом или отдельных нарушениях.
В психическом состоянии выявлялись проявления брадипсихизма с замедленностью темпа мышления и речи, трудности концентрации внимания, его неустойчивость и истощаемость, что отчетливо обнаруживалось при тестировании и проявлялось трудностями удержания программы деятельности, отвлекаемостью, забыванием задания, замедленным темпом выполнения. При этом пациенты охотно подвергались процедуре тестирования, а замечая свои ошибки или при указании на недочеты, сокрушались или грустно иронизировали по поводу ослабления памяти или сообразительности. Начальные проявления трудностей называния предложенных предметов или изображений компенсировались заменой или описанием их назначения, при этом минимальная звуковая подсказка быстро приводила к нужному результату. Запинки и паузы при подборе слов, замедленность речи сочетались с обстоятельностью и излишней детализацией, увязанием в подробностях или с неоднократным повторением уже сказанного. Эмоциональная лабильность проявлялась эпизодами слезливого слабодушия на фоне преимущественно благодушного фона настроения или возникновением тревожности на фоне пониженного настроения.
Основные клинические и демографические параметры в исследованной группе больных представлены в табл.1.
Таблица 1
Общая характеристика больных с синдромом MCI церебрально-сосудистого генеза до лечения АктовегиномПараметры Число больных Пол:
— мужской
— женский
23Средний возраст (лет) Средний возраст начала заболевания (лет) Длительность заболевания Средние суммарные оценка по шкалам (баллы) до начала терапии:
— шкала Хачински
— MMSE
26,8 ±1,2При магнитно-резонансном исследовании (МРТ) головного мозга до начала терапии у подавляющего большинства пациентов выявлены томографические признаки гидроцефалии: расширение субарахноидальных пространств — у 25 пациентов из 30 (83,3%) и увеличение желудочков мозга — у 26 пациентов (86,7%). У 18 больных (60,0%) обнаружены постишемические очаги небольшого объема, расположенные перивентрикулярно: единичные до 1,5 см в диаметре — у 7 больных (23,3%) или множественные мелкие — у 11 больных (36,7%). Лейкоареоз отмечен в 19 случаях (63,3%). В целом, по данным МРТ, признаки сосудистой энцефалопатии нашли свое подтверждение почти у всех пациентов.
У включенных в исследование пациентов определен полиморфизм генотипа аполипо-протеина (ApoE) по анализу крови. В двух третях наблюдений пациенты имели АроЕ 4(-) генотип со следующим распределением ε2 и ε3 аллелей: 3.3,3.2,2.3 (соответственно 51,9, 3,7 и 11,1%). 7 больных (25,9%) имели АроЕ 4(+) генотип, в том числе 3.4,4.4 и 2.4 (соответственно 25,9, 3,7 и 3,7%). У включенных в исследование пациентов выявлены различные виды соматической патологии (табл. 2). 80% больных страдали артериальной гипертензией. Более чем у половины больных диагностировалась ишемическая болезнь сердца, в одной трети этих случаев отмечались нарушения проводимости и ритма сердца.
Таблица 2
Частота соматической патологии в исследованной группе больныхСоматическая патология Артериальная гипертензия Артериальная гипотония ИБС (кардиосклероз) НК1 ЭКГ (замедление в/ж проводимости, неполная блокада правой или левой ветвей п. Гиса, передней ножки п. Гиса) Мерцательная аритмия Хронический гастрит Хронический энтероколит Хронический панкреатит Сахарный диабет РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Клиническая положительная динамика в психическом состоянии пациентов отмечалась, как правило, к концу курсового лечения Актовегином. Существенно уменьшался объем жалоб больных, в том числе выраженность или урежение головных болей (пациенты отмечали, что «в голове просветлело», «прибавилось сил»). Ощущение головокружения, по их признанию, возникало заметно реже, исчезала шаткость походки, неустойчивость равновесия. В ряде случаев отмечалось и уменьшение тягостного ощущения шума в голове или в ушах. Больные также отмечали улучшение ночного сна, уменьшение утомляемости, возрастание активности и работоспособности. Улучшение настроения сопровождалось снижением уровня тревожности, дезактуализацией сверхценных опасений, (по словам больных, «как будто надели фильтр»). При сохранении забывчивости больные обнаруживали меньшую склонность к фиксации на этих проявлениях.
Обращало на себя внимание, что уже со второй недели лечения у пациентов, в состоянии которых до начала терапии отмечались признаки субдепрессии или отдельные депрессивные симптомы, улучшался общий фон настроения, причем эта положительная динамика сохранялась до конца курсового введения Актовегина и даже спустя месяц по его окончании.
Наряду с уменьшением жалоб, редукцией астенических расстройств, восстановлением или возрастанием эмоциональной устойчивости существенную положительную динамику претерпевали нарушения когнитивного функционирования. В первую очередь это относится к улучшению концентрации внимания и уменьшению заторможенности. Ускорение темпа психической деятельности проявлялось в более быстрых ответах на вопросы, улучшении темпа деятельности при выполнении тестовых заданий. В части случаев отчетливым было уменьшение торпидности мышления и проявлений брадипсихизма в целом. Возрастала активность и инициативность в беседе и общении, восстанавливалась повседневная деятельность в необходимом объеме. Уменьшались проявления речевых затруднений, в спонтанной речи исчезали запинки и паузы, пациенты быстрее и лучше справлялись с называнием. Дисмнестические расстройства заметно уменьшались в своей выраженности, что находило свое отражение в увеличении объема запоминания или в большей легкости воспроизведения упроченной информации. Следует подчеркнуть, что лечение Актовегином отчетливо влияло на восстановление скорости психических процессов и общий уровень когнитивного функционирования. Важно отметить, что этот эффект оказался достаточно устойчивым и сохранялся спустя месяц после завершения терапии Актовегином, когда пациенты не получали никакого другого лечения, кроме поддерживающей терапии соматических заболеваний.
Оценка эффективности терапии по шкале общего клинического впечатления (CGI)
Улучшение общего клинического состояния в исследованной группе больных к 14-му дню терапии отмечено в 96,7% случаев, включая минимальное улучшение у 73,4% больных и умеренное улучшение у 23,3% пациентов (рис. 1). У 1 пациента к 14-му дню лечения состояние незначительно ухудшилось.
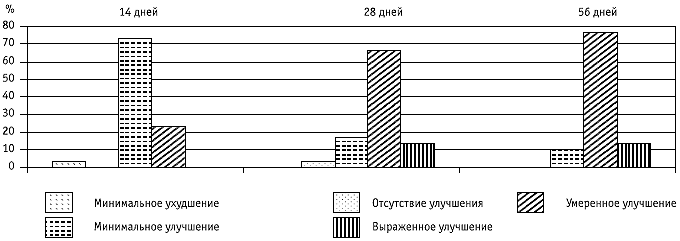
Рис. 1. Эффективность терапии Актовегином по шкале CGI-ImprovementК моменту завершения курса терапии (28 дней лечения) общая частота улучшения различной степени выраженности оставалась той же (96,7%), однако уже у 66,7% больных было установлено умеренное улучшение, у 13,3% больных достигнуто выраженное улучшение и только у 16,7% пациентов отмечено минимальное улучшение. У 1 пациента состояние не изменилось.
Спустя 28 дней после окончания курса лечения частота улучшения различной степени выраженности составляла 100%. Умеренное улучшение отмечено у 76,7% больных, выраженное улучшение было установлено в 13,3% случаев, минимальное улучшение — в 10% случаев.
Оценка терапевтической динамики состояния когнитивных функций по шкале MMSE
По шкале MMSE отмечено статистически достоверное улучшение (p < 0,01) когнитивных функций на каждом из этапов курса терапии (спустя 14 дней и к моменту окончания курса лечения — 28 дней) по сравнению с исходным уровнем (табл. 3, рис. 2). Спустя 28 дней после окончания лечения (оценка на 56-й день исследования) улучшение средней групповой оценки по сравнению с исходной оставалось на статистически достоверном уровне (p < 0,01).
Таблица 3
Динамика средних показателей (M ± SD) оценки когнитивных функций по шкале MMSE* Различия достоверны по сравнению с оценкой до начала терапии (р < 0,01).
Рис. 2. Улучшение состояния когнитивных функций по шкале MMSEОценка терапевтической динамики состояния по тесту «Вербальные ассоциации»
По тесту «Вербальные ассоциации» статистически достоверное увеличение количества называемых в течение 1 минуты слов (начинающихся на букву «к») по сравнению с исходным уровнем (p < 0,01) отмечено и к середине (14 дней), и к окончанию курса терапии (28 дней) (табл. 4, рис. 3). При этом к 56-му дню исследования (через 28 дней после завершения курса лечения) суммарная оценка по шкале оказалась даже более высокой по сравнению с оценкой к моменту окончания курса терапии.
Таблица 4
Динамика средних показателей (M ± SD) по тесту «Вербальные ассоциации»День оценки Количество слов (среднегрупповое значение) * Различия достоверны по сравнению с оценкой до начала терапии (р < 0,01).
Рис. 3. Улучшение средних показателей по тесту «Вербальные ассоциации»Оценка терапевтической динамики состояния когнитивных функций по Шкале лобной дисфункции
Статистически достоверное улучшение (p < 0,01) отмечено по тестам «Концептуализация» и «Звуковые ассоциации» — к 14-му и 28-му дням курса лечения, а также к 56-му дню исследования, то есть спустя 28 дней после окончания введения Актовегина (табл. 5). Оценки по тестам «Простая реакция выбора» и «Усложненная реакция выбора» достигали статистически достоверного значения ко времени окончания курса лечения (p < 0,01). Улучшения суммарной оценки по тесту «Динамический праксис» не произошло.
Таблица 5
Динамика средних показателей (M ± SD) по Шкале лобной дисфункцииТесты Концептуализация Звуковые ассоциации Динамический праксис Простая реакция выбора Усложненная реакция выбора Суммарная оценка
* Различия достоверны по сравнению с оценкой до начала терапии (р < 0,01).Статистически достоверное улучшение суммарной оценки по Шкале лобной дисфункции отмечено на каждом этапе курса терапии (14-й и 28-й дни) по сравнению с исходным уровнем (табл. 6) и оставалось на статистически достоверном уровне спустя 28 дней после окончания лечения.
Таблица 6
Динамика средних показателей (M ± SD) по Тесту рисования часовДень оценки Суммарная оценка
* Различия достоверны по сравнению с оценкой до начала терапии (р < 0,01).Оценка терапевтической динамики по Тесту рисования часов
Оценка по Тесту рисования часов статистически достоверно улучшалась (p < 0,01) на каждом из этапов курса терапии (14-й и 28-й дни) по сравнению с исходным уровнем (табл. 6). Улучшение оставалось статистически достоверным и через 28 дней после окончания лечения.Оценка терапевтической динамики по Бостонскому тесту называния
Суммарное групповое количество самостоятельных правильных ответов по Бостонскому тесту называния статистически достоверно улучшалось (p < 0,01) на каждом из этапов курса терапии (14-й и 28-й дни) по сравнению с исходным уровнем (табл. 8). Улучшение оставалось статистически достоверным также и через 28 дней после окончания лечения.
Таблица 7
Динамика среднего показателя количества самостоятельных правильных ответов (M ± SD) по Бостонскому тесту называнияДень оценки Количество самостоятельных правильных ответов (суммарная оценка)
*Различия достоверны по сравнению с оценкой до начала терапии (р < 0,01).Оценка терапевтической динамики состояния когнитивных функций по Шкале деменции Маттиса
По тестам «Сходства» и «Память» статистически достоверное улучшение (p< 0,01) отмечено к 14-му и 28-му дням курса лечения, а также через 4 недели катамнеза (табл. 8). Улучшения суммарных оценок по тестам «Реципрокная координация» и «Графомоторная проба» не отмечено.
Таблица 8
Динамика средних показателей (M ± SD) по Тесту деменции МаттисаТесты Реципрокная координация Графомоторная проба Сходства Память
*Различия достоверны по сравнению с оценкой до начала терапии (р < 0,01).Оценка терапевтической динамики по Тесту запоминания 10 слов
По Тесту запоминания 10 слов статистически достоверное улучшение суммарных оценок при первой, второй и третьей попытках запоминания слов (p < 0,01) отмечено к 14-му и 28-му дням курса лечения, а также к 28-му дню катамнеза (табл. 9).
Таблица 9
Динамика средних показателей (M ± SD) по Тесту запоминания 10 словПоказатели Непосредственное воспроизведение 1-я попытка 2-я попытка 3-я попытка Отсроченное воспроизведение
* Различия достоверны по сравнению с оценкой до начала терапии (р < 0,01).Статистически достоверное улучшение суммарной оценки отстроченного воспроизведения слов достигнуто к 28-му дню терапии. Статистически достоверный уровень ее улучшения сохранялся и через 4 недели катамнестического наблюдения, хотя степень улучшения суммарной оценки несколько уменьшилась.
Эффективность терапии по шкале депрессии Гамильтона
По шкале депрессии Гамильтона статистически достоверное улучшение суммарной групповой оценки (p < 0,01) отмечено к 14-му и 28-му дням курса лечения, а также к 28-му дню катамнеза (табл. 10, рис. 4). Абсолютное значение улучшения суммарной оценки к 14-му дню терапии составило 3,0 балла, к 28-му дню — 4,9 балла. Спустя 28 дней после завершения курса лечения достигнутое к 28-му дню терапии улучшение суммарной оценки сохранялось на уровне 4,9 балла.
Таблица 10
Динамика средних показателей (M ± SD) по шкале депрессии ГамильтонаДень оценки Суммарная оценка
* Различия достоверны по сравнению с оценкой до начала терапии (р < 0,01).
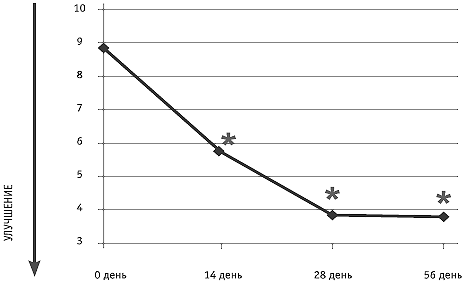
* Различия достоверны по сравнению с оценкой до начала терапии (р < 0,01).
Рис. 4. Динамика средних показателей (M ± SD) по шкале депрессии Гамильтона * Различия достоверны по сравнению с оценкой до начала терапии (p < 0,01).Нежелательные явления на лечении Актовегином во время проведения исследования отсутствовали.
ОБСУЖДЕНИЕ ПОЛУЧЕННЫХ РЕЗУЛЬТАТОВ
Результаты проведенного открытого неконтролируемого исследования эффективности курсового лечения Актовегином при ежедневном внутримышечном введении препарата в дозе 200 мг продемонстрировали значительное улучшение в состоянии подавляющего большинства пациентов с синдромом MCI церебрально-сосудистого генеза. Отмечено достоверное улучшение среднегрупповых показателей практически по всем тестам, использованным для оценки когнитивных дисфункций. Следует отметить несомненное воздействие препарата в изученной лекарственной форме на улучшение концентрации внимания, ускорение темпа психической деятельности и процессы запоминания.
Полученные данные соответствуют приводимым в литературе указаниям на улучшение когнитивных функций при ДЭ с признаками цереброваскулярной недостаточности под влиянием лечения Актовегином [7; 8; 10; 17; 19]. В частности, показано, что энцефалотропные эффекты Актовегина, улучшение вигильности, по данным ЭЭГ, наиболее выражены в теменной, фронтоцентральной и височно-затылочной областях, где, по показателям ПЭТ, снижен кровоток и транспорт глюкозы.
Требования к эффективности лечения когнитивных нарушений [15] предполагают положительное воздействие на скорость осуществления когнитивных процессов, на процессы кратковременной и среднесрочной памяти и общее самочувствие пациентов. Фармакологические свойства Актовегина обеспечивают возможность удовлетворения этих требований и определяют показания к назначению Актовегина при синдроме MCI церебрально-сосудистого генеза.
Хотя не приходится обоснованно судить об антидепрессивных свойствах препарата, но нельзя обойти вниманием тот факт, что при лечении Актовегином наблюдалось уменьшение выраженности или исчезновение депрессивных симптомов, тем более что никто из пациентов не получал антидепрессивной терапии в период лечения Актовегином.
Особый интерес представляет тот факт, что положительный терапевтический эффект продолжал нарастать и по окончании курса терапии Актовегином, что свидетельствует не только о стойкости улучшения, но и о возможном его воздействии на мобилизацию компенсаторных механизмов.
Ни у одного из пациентов не отмечалось нежелательных явлений при внутримышечном введении Актовегина.
ВЫВОДЫ
1. Внутримышечное курсовое введение Актовегина (по 200мг/сутки №28) эффективно для лечения синдрома MCI церебрально-сосудистого генеза у пациентов пожилого возраста.
2. Актовегин положительно воздействует как на общее клиническое состояние и когнитивное функционирование пациентов, так и на отдельные составляющие когнитивных дисфункций: ассоциативное мышление, различные компоненты мнестической функции — зрительную и слухоречевую память, номинативную функцию речи, произвольное запоминание в слухоречевой сфере, а также на динамический праксис и произвольную регуляцию праксиса, зрительно-пространственную деятельность.
3. Актовегин, кроме того, уменьшает выраженность депрессивных симптомов у этого контингента больных.
4. Отсутствие нежелательных явлений свидетельствует о безопасности проведения курсового лечения Актовегином по применявшейся методике у пациентов пожилого и старческого возраста.
5. Эффективность и безопасность внутримышечного введения Актовегина определяет перспективу более широкого использования препарата в амбулаторной гериатрической практике у пациентов с легкими когнитивными нарушениями сосудистого генеза.ЛИТЕРАТУРА
1. Гаврилова С.И., Калын Я. Б., Сударева Л.О. Эпидемиология деменций пожилого и старческого возраста// Журн. невропатол. и психиатр. — 1987. — №9.— С. 44-50.
2. Гаврилова С.И. Фармакотерапия болезни Альцгеймера. — М.: Пульс. — 360 с.
3. Дамулин И. В. Сосудистые легкие когнитивные нарушения // Психиатр. и психофармакотер. — 2005. — Т. 7, №5. — С. 295-299.
4. Захаров В. В., Яхно Н. Н. Синдром умеренных когнитивных расстройств в пожилом возрасте: диагностика и лечение // РМЖ. — 2004. — Т. 12, №10. — С. 573-577.
5. Калын Я.Б., Гаврилова С.И. Динамика показателей распространенности психических расстройств в населении пожилого и старческого возраста/Реформы службы психического здоровья: проблемы и перспективы. — М., 1997. — С. 181-189.
6. Летцел Х., Шиктигер У. Применение актовегина у пожилых пациентов с органическим синдромом // РМЖ. — 2003. — Т. 11, №25.— С. 1428-1431.
7. Михайлова Н. М., Кладова А. Ю. Проблема психоорганического синдрома в амбулаторной психиатрии // Болезнь Альцгеймера и старение: от нейробиологии к терапии. — М., 1999. — С. 74-82.
8. Остроумова О.Д., Боброва Т.А. Когнитивные нарушения и деменция: возможности терапии препаратом Актовегин // Сердце. — 2003. — Т. 2, №4. — С. 210-214.
9. Рощина И.Ф., Гаврилова С.И., Михайлова Н.М. и др. Нейропсихологическое проспективное исследование больных с так называемой сомнительной деменцией // Психиатрия. — 2003. — №4.— С. 54-57.
10. Херман В.М., Бон-Щечевский В.Дж., Кунтц Г. Инфузионная терапия актовегином у пациентов с первичной дегенеративной деменцией типа Альцгеймера и мультиинфарктной деменцией (результаты проспективного плацебо-контролируемого двойного слепого исследования у пациетов, находящихся в условиях стационара) // РМЖ. — 2002. — Т. 10, № 15. — С. 658-663.
11. Шахпаронова Н.В., Кадыков А. С. Нейрометаболическая терапия больных с заболеваниями нервной системы. Возможности применения Актовегина // РМЖ. — 2008. — Т. 16, №26. — С. 1722-1725.
12. Шмидт Е.В. Классификация сосудистых поражений головного и спинного мозга// Журн. невропатол. и психиатр. — 1985. — №9.— С. 1281-1288.
13. Шмырев В. И., Остроумова О.Д., Боброва Т.А. Возможности препарата актовегин в профилактике и лечении деменции // РМЖ. — 2003. — Т. 11, №4.— С. 216-220.
14. Янсен В.. Брукнер Г. В. Лечение хронической цереброваскулярной недостаточности с использованием драже актовегин-форте (двойное слепое плацебо-контролируемое исследование) // РМЖ. — 2002. — Т. 10, №12-13. — С. 543-546.
15. Kanowsky S., Kinzler E., Lehman E. et al. Confirmed clinical efficacy of actovegin in elderly patients with organic brain syndrome // Pharmacopsychiat. — 1995. — Vol. 28. — P. 125-133.
16. Lopez O., Jagust W., De Cosky S. et al. Prevalence and Classification of Mild Cognitive Impairment in the Cardiovascular Health Study// Arch. Neurol. — 2003. — Vol. 60, №10. — P. 1385-1389.
17. Meyer A. Is Mild Cognitive Impairment Prodromal for Vascular Dementia Like Alzheimer's Disease?// Stroke. — 2002. — Vol. 33. — P. 1981-1985.
18. Oswald W. D., Steger W., Oswald B. et al. Die Verbesserung fluider Kognitiver Leistungen als Indikator fur die Klinische Wirksamkeit einer nootropen Substanz. Eine placebokontrolierte Doppelblind-Studie mit Actovegin // Z. Gerontopsychol.-Psychiatr. — 1991. — Bd. 4.—S. 209-220.
19. Oswald W. D., Steger W., Oswald B. et al. Die Verbesserung fluider Kognitiver Leistungen mit Actovegin-Infusionen bei Alterpatienten mit leichtem bis mittel-schwerem organischem Psychosyndrom // Z. Gerontopsychol.-Psychiatr. — 1992. — Bd. 5.—S. 251-266.
20. Reisberg B., Ferris S. H., de Leon M.J.etal. The global deterioration scale for assessment of primary degenerative dementia // Fm.J. Psychiatry, 1982. — Vol. 139. — P. 1136-1139.
21. Saletu B., Gruenberger J., Linzmayer L. et al. EEG brain mapping and psychometry in age-associated memory impairment after 2 weeks infusions with the hemoderivative Actovegin: double blind placebo controlled trials // Neuropsychobiol. — 1991. — Vol. 24. — P. 135-145.
| Апрель 2010 г. |