Опубликовано в журнале:
ИНСУЛЬТ, 18, 2006Рандомизированное двойное слепое плацебо-контролируемое исследование эффективности и безопасности мексидола в комплексной терапии ишемического инсульта в остром периоде
В.И. CKBOPЦOBA, Л.В. СТАХОВСКАЯ, Я.P. НАРНИССОВ, М.К. БОДЫХОВ, И.В. КИЧУК, Ю.В. ГУДКОВА, Т.Д. СОЛДАТЕНКОВА, Т.Т. КОНДРАШОВА, Е.В. КАЛИНИНА, М.Д. НОВИЧКОВА, О.Б. КЕРБИКОВ
The randomized double-blind placebo-controlled study of efficacy and safety of mexidol in the complex therapy of ischemic stroke in the acute period
V.I. SKVORTSOVA, L.V. STAKHOVSKAYA, YA.R. NARTSYSSOV, M.K. BODYKHOV, I.V. KICHUCK, YU.V. GUDKOVA, T.D. SOLDATENKOVA, T.T. KONDRASHEVA, E.V. KAUNINA, M.D. NOVICHKOVA, O.B. KERBIKOVКафедра фундаментальной и клинической неврологии Российского государственного медицинского университета; НИИ цитохимии и молекулярной фармакологии, Москва
В исследование были включены больные с ишемическим инсультом в возрасте 45-85 лет (51 человек), поступившие в первые 24 ч от начала заболевания. Мексидол вводили в дозе 300 мг/сут 24 больным в течение 14 сут от начала инсульта. Плацебо вводили 27 больным по аналогичной схеме. Выявлены достоверная опережающая динамика в регрессе неврологических нарушений по шкале NIH к 14-м суткам заболевания в группе больных, получавших мексидол по сравнению с группой плацебо (р<0,05), а также достоверное функциональное восстановление (динамика клинического балла по шкале Бартел на 21-е сутки; р<0,05) у больных, включенных в исследование в первые 6 ч заболевания. Установлена нормализация функциональной активности мозга при лечении мексидолом, в том числе при проведении острой фармакологической пробы. Комплекс исследований антиоксидантной системы выявил повышение активности ее ферментов (супероксиддисмутазы, глутатионпероксидазы, глутатионредуктазы) при введении мексидола по сравнению с плацебо. При анализе ферментов дыхательной цепи митохондрий отмечено повышение активности сукцинатдегидрогеназы. Таким образом, получено достоверное клиническое подтверждение эффективности мексидола в остром периоде ишемического инсульта в каротидной системе атеротромботического или кардиоэмболического патогенетического типа, особенно при раннем (до 6 ч) его назначении; уточнены механизмы действия препарата (антигипоксические, антиоксидантные) в клинических условиях.
Ключевые слова: ишемический инсульт, мексилол.
The first randomized double-blind placebo-controlled study of efficacy of mexidol has been conducted. Fifty-one patients with ischemic stroke, aged 45-85 years, admitted during the first 24 hours after stroke were switched to mexidol in dosage 300 mg daily during 14 days. Twenty seven patients received the placebo using the same scheme. The significant forward dynamics in regress of neurological disturbances on the NIH scale was found to the 14th day in patients treated with mexidol as compared to the placebo group (p<0.05), along with functional rehabilitation assessed according to the dynamics of clinical scores on the Bartel scale to the 21st day after stroke (p<0.05) in patients involved in the study during the first 6 hours after disease onset. The normalization of functional brain activity was revealed in patients receiving mexidol, in comparison with the placebo, i.e. during the acute pharmacological test. A study of the antioxidant system demonstrated the increase of enzyme activity (superoxide dismutase, glutathione peroxidase, glutathione reductase) and the analysis of enzyme activity of the respiratory mitochondrial chain revealed the increase of succinate dehydrogenase activity in patients receiving mexidol. The results confirm the clinical efficacy of mexidol in the acute period of ischemic stroke in the carotid system of atherothrombotic or cardioembolic pathogenetic types, especially for its earlier (up to 6 hours) prescription, and specify mechanisms of its action (antihypoxic antihypoxic, antioxidant) in clinical conditions.
Key words:
Широкая распространенность инсульта, значительная частота его развития, высокий процент инвалидизации и смертности обусловливают высокую медицинскую и социальную значимость проблемы, необходимость дальнейшего изучения патогенетических механизмов и поиск новых подходов к диагностике и лечению этого заболевания [1].
Проведенные в конце XX века исследования патогенеза ишемического инсульта кардинально изменили тактику ведения пациентов в его остром периоде, определив патогенетические механизмы формирования ишемии и возможные пути ее коррекции [1].
Одним из основных механизмов повреждения клеток при ишемии является оксидантный стресс. Наличие в ЦНС большого количества липидных соединений, а также относительно низкая активность антиоксидантных систем объясняют наибольшую подверженность головного мозга оксидантному повреждению [1]. В его развитии безусловную роль играет гипоксия, возникающая при локальном нарушении мозгового кровотока. Наряду с этим наличие коллатералей, спонтанная или индуцированная реканализация окклюзированного сосуда могут приводить к постишемической гиперемии. Наблюдаемый при этом избыток кровотока не соответствует метаболическим потребностям ткани мозга и также способен инициировать новую волну оксидантного повреждения клеток [1].
В последнее десятилетие в ряде экспериментальных работ [2] и открытых исследований [3- 5] обоснована эффективность применения мексидола, являющегося антиоксидантом - антигипоксантом прямого действия.
Целью настоящей работы явилось рандомизированное двойное слепое плацебо-контролируемое исследование эффективности и безопасности мексидола в остром периоде ишемического инсульта.
Материал и методы
В исследование был включен 51 пациент с ишемическим инсультом в каротидной системе, которые поступили в отделение нейрореанимации в первые 24 ч от начала заболевания. Возраст их варьировал от 45 до 85 лет (средний 69,6±9,8 года). Мужчин было 21 (41%), женщин - 30 (59%).
Критериями исключения являлись наличие геморрагического инсульта, инсульта в вертебрально-базилярной системе, повторных инсультов, острого инфаркта миокарда, выраженной сердечной, почечной или печеночной недостаточности, анемии и других заболеваний, сопровождающихся нарушением системной гемодинамики и метаболизма, а также участие в других исследованиях.
В соответствии с классификацией TOAST у 29 (56,9%) больных был атеротромботический патогенетический вариант развития инсульта, у 22 (43,1%) - кардиоэмболический. Пациенты с лакунарным (микроциркуляторным) инсультом в исследование не включались.
Из общего числа обследованных у 23 (45%) имела место левополушарная локализация очага поражения мозга, у 18 (35%) - правополушарная.
Методом простой рандомизации и вслепую пациентов разделили на две группы. В одной из них (24 пациента - 13 мужчин и 11 женщин, возраст 65,8±9,6 года) вводили мексидол в дозе 300 мг/сут: в первые 3 сут внутривенно капельно на 200 мл физиологического раствора, затем внутримышечно по 100 мг (2,0 мл 5% раствора) 3 раза в сутки до 14-х суток от начала заболевания. В другой группе (27 пациентов - 8 мужчин и 19 женщин, возраст 73±8,9 года) по такой же схеме применяли плацебо.
Учитывая эффективность глицина, доказанную в ходе рандомизированного двойного слепого плацебо-контролируемого исследования [6], всем пациентам в остром периоде заболевания его назначали по 1 г в сутки сублингвально. Кроме того, всем пациентам проводили максимально унифицированную базисную терапию в соответствии с рекомендациями Европейской инициативной группы по проблеме инсульта [7].
Для объективизации тяжести состояния, выраженности очагового неврологического дефицита и оценки динамики клинических показателей использовали балльную шкалу NIH при поступлении больного в клинику (до начала терапии), на 3, 7 и 14-е сутки инсульта. Степень функционального восстановления определяли по шкале Бартел на 21-е сутки инсульта.
У всех больных регистрировали ЭЭГ на приборе EEG-24 (фирма МБН, Москва). Использовали монополярный монтаж 19 активными электродами, располагавшимися на коже головы по международной системе 10-20, относительно раздельных референтных ушных электродов.
Электроэнцефалографию проводили в 1-е, на 3, 7 и 14-е сутки. В 1-е сутки ЭЭГ записывали до и после введения препарата в течение 150 мин от начала терапии. Для оценки биоэлектрической активности головного мозга использовали соотношение мощности медленной и быстрой активности (М/Б), мощности α-активности в передних и задних отделах полушарий (Ап/Аз), индексы ритмов.
Учитывая преимущественно антиоксидантную направленность действия мексидола, у всех больных исследовали состояние антиоксидантной системы. Определяли активность супероксиддисмутазы (СОД), каталазы, глутатионпероксидазы (ГПО) и глутатионредуктазы (ГР), концентрацию восстановленного глутатиона (Г-SH) и вторичных продуктов перекисного окисления липидов, реагирующих с тиобарбитуровой кислотой (ТБКРП). Для этого брали кровь из локтевой вены в вакуумные пробирки, содержавшие гепарин, в 1-е сутки заболевания (до начала терапии), на 3, 7 и 14-е сутки.
Активность ферментов определяли спектрофотометрически (спектрофотометр SPE-CORD W-VIS), рассчитывая на 1 мг гемоглобина, концентрацию которого в гемолизате исследовали гемоглобинцианидным методом.
Для оценки влияния мексидола на клеточное дыхание использовали цитохимические методы определения активности сукцинатдегидрогеназы (СДГ), α-глицерофосфатдегидрогеназы митохондрий (α-ГФДГ) и щелочной фосфатазы (ЩФ). Для этого в 1-е сутки заболевания, на 3, 7 и 14-е брали капиллярную кровь, приготовленные мазки высушивали и фиксировали в течение 30 с 10% раствором спирт-формалина для определения активности ЩФ или раствором ацетона, насыщенным трилоном Б, для определения активности СДГ и α-ГФДГ. При оценке активности ферментов мазки окрашивали методом азосочетания для ЩФ и методом Р.П. Нарциссова (с помощью солей тетразолия) для СДГ и α-ГФДГ. После этого проводили микрокопирование мазков под масляной иммерсией.
В мазке подсчитывали 100 клеток с подразделением их на 5 групп:
0/0: отсутствие фермента
1/+: низкая активность, при этом цитоплазма имеет нежное диффузное прокрашивание или на фоне такого прокрашивания отмечаются единичные гранулы
2/++: умеренная реакция, при которой количество гранул и степень диффузного прокрашивания более выражены, но между гранулами имеются просветы
3/+++: высокая активность: в цитоплазме имеются гранулы, едва различимые на фоне сильного диффузного прокрашивания, но ядро клетки хорошо просматривается
4/++++: очень высокая активность, при этом ядро не определяетсяУсловную единицу активности фермента вычисляли по P. Kaplow (1955): количество клеток в каждой группе умножали на ее номер, затем полученные произведения суммировали. Сумма является показателем активности фермента.
Группа контроля включала 27 практически здоровых добровольцев (средний возраст 64,4±5,2 года); - 12 (44%) мужчин и 15 (56%) женщин.
Статистическую обработку результатов проводили с помощью программы STATISTICA-6.0. На первом этапе обработки совокупностей данных использовали тест на нормальность распределения. Поскольку распределение большинства совокупностей данных отличалось от нормы, достоверность различий устанавливали с помощью непараметрического U-критерия Манна- Уитни. Летальность оценивали с помощью критерия χ2 с поправкой Йетса. Если хотя бы одно из ожидаемых значений в таблице сопряженности было менее 5, для анализа использовали односторонний вариант точного критерия Фишера. Ранговые коэффициенты корреляции рассчитывали по Спирмену.
Результаты и обсуждение
При анализе динамики клинического балла по шкале NIH (рис. 1) выявлялось опережение восстановления нарушенных неврологических функций у пациентов, получавших мексидол (более выраженное снижение суммарного клинического балла), по сравнению с получавшими плацебо. При этом достоверные (p<0,05) различия между группами определялись к окончанию курсового введения препарата - 14-м суткам.
Рис. 1. Динамика клинического балла по шкале NIH.
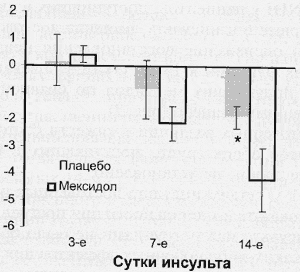 Примечание. Здесь и на рис. 2: * - достоверные различия между группами (р<0,05).
Примечание. Здесь и на рис. 2: * - достоверные различия между группами (р<0,05).Анализ сроков включения пациентов в исследование показал следующее. В группе получавших мексидол и в группе получавших плацебо выявлено по 17 пациентов, включенных в исследование в первые 6 ч инсульта. От 6 до 12ч в группу плацебо были включены 8 пациентов, в группу мексидола - 5. В сроки от 12 до 24 ч от начала заболевания в исследование были включены по 2 человека каждой из групп.
При анализе клинической картины инсульта у включенных в исследование в первые 6 ч и получавших мексидол больных определялся достоверно более высокий клинический балл по шкале NIH (более тяжелое клиническое состояние) в 1-е и на 3-й сутки инсульта по сравнению с пациентами, получавшими плацебо (табл. 1).
Таблица 1. Динамика клинического балла по шкале NIH и степень восстановления по шкале Бартела у больных, поступивших в клинику в первые 6 ч развития инсульта
Группа Балл по NIН Балл по шкале Бартела сутки 1-е 3-и 7-е 14-е 21-е Плацебо 10,8±6 11,1±6,1 10,1±6,2 9,1±6,1 58,0 Мексидол 15,6±6* 16,4±7,5* 13±8,1 10,5±7,3 72,5* Примечание. * - достоверные различия между группами (p<0,05).Обращают на себя внимание отсутствие достоверных различий между группами на 7-е и 14-е сутки, а также достоверно больший балл по шкале Бартела на 21-е сутки у пациентов, получавших мексидол.
Оценка динамики клинического балла по шкале NIH у пациентов, поступивших в клинику в первые 6 ч инсульта, выявила достоверное (p<0,05) опережение восстановления неврологических функций к 14-м суткам заболевания в группе получавших мексидол по сравнению с получавшими плацебо (рис. 2).
Рис. 2. Динамика клинического балла по шкале NIH у больных, поступивших в клинику в первые 6 ч развития инсульта.
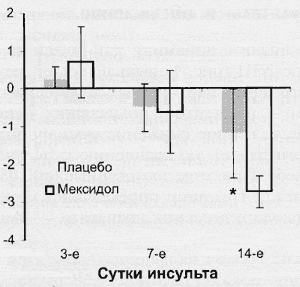
Достоверных различий в тяжести состояния пациентов обеих групп, поступавших в более поздние сроки, не установлено.
К 21-м суткам инсульта достоверных различий в показателях летальности при прогредиентном инсульте между группами не было обнаружено. Каких-либо побочных эффектов при внутривенном или внутримышечном введении мексидола не отмечалось.
При анализе показателей биоэлектрической активности мозга в ходе проведения острой фармакологической пробы установлено, что у пациентов, получавших плацебо, в течение 150 мин регистрации ЭЭГ после его первого введения увеличился индекс 9-активности (достоверно по сравнению с группой больных, получавших мексидол, в непораженном полушарии; p<0,05) и уменьшилась частота α-ритма в затылочных отведениях (достоверно по сравнению с группой больных, получавших мексидол, в непораженном полушарии; p<0,005). Отмечались тенденция к уменьшению индекса α-ритма в обоих полушариях и перераспределение мощности α-ритма с увеличением его представленности в переднецентральных отведениях (достоверно по сравнению с группой больных, получавших мексидол, в обоих полушариях увеличился индекс Ап/Аз; p<0,05). В группе плацебо также было выявлено увеличение представленности медленной активности по отношению к быстрой (достоверно по сравнению с группой больных, получавших мексидол, увеличился индекс М/Б в обоих полушариях; p<0,05). В группе получивших мексидол показатели биоэлектрической активности в течение 150 мин после первого введения препарата оставались стабильными (табл. 2).
Таблица 2. Некоторые показатели ЭЭГ при проведении острой фармакологической пробы (регистрации ЭЭГ до и спустя 150 мин после введения препарата)
Показатель Плацебо Мексидол до введения препарата через 150 мин Р до введения препарата через 150 мин Р Частота α-ритма, Гц А 1 1,05±0,22 А 11,03±0,23 <0,48 А 11,13±0,16 А 11,16±0,22 <0,30 Б 11,05±0,29 Б 10,96±0,29 <0,001 Б 11,09±0,18 Б 1 1,07±0,19 <0,61 Ап/Аз А 1,79±0,96 А 2,32±1,42 <0,02 А 1,94±1,47 А 1,92±1,24 <0,88 Б 1,92±1,58 Б 2,35 ± 1,64 <0,03 Б 1,99±1,19 Б 2,29±1,55 <0,22 Индекс θ-активности А 0,38±0,14 А 0,41±0,15 <0,11 А 0,44±0,12 А 0,42±0,12 <0,16 Б 0,30±0,11 Б 0,33±0,14 <0,01 Б 0,37±0,13 Б 0,35±0,10 <0,29 М/Б А 2,64±1,95 А 3,08±2,55 <0,04 А 2,67±1,62 А 2,61 ± 1,39 <0,77 Б 1,21±0,84 Б 1,60±1,15 <0,02 Б 1,42±0,81 Б 1,36±0,83 <0,70 МПАД, % 0,20±0,37 0,18±0,39 <0,85 0,07±0,87 0,13±0,72 <0,75 МПАТ, % 41,11±36,91 49,94±42,7 <0,05 41,91±28,3 42,06±31,8 <0,97 Примечание. Здесь и в табл. 3: А - пораженое полушарие, Б - интактное полушарие. МПА - межполушарная асимметрия.Выявленные изменения в группе пациентов, получавших плацебо, и относительная стабильность показателей в течение 150 мин регистрации ЭЭГ в группе получавших мексидол отражают нормализующее влияние этого препарата на функциональную активность структур головного мозга подкорково-диэнцефального уровня, что может свидетельствовать о его антигипоксической направленности.
Достоверные различия в динамике показателей биоэлектрической активности между группами больных выявлены на 3-й сутки заболевания. В группе мексидола отмечены нормализация распределения а-ритма в непораженном полушарии (p<0,05) и достоверное снижение показателя Ап/Аз по сравнению с 1-ми сутками. К 14-м суткам значения этого показателя составили 0,66 в группе мексидола и 1,5 в группе плацебо (p<0,005). Индекс θ-ритма в группе мексидола снижался, начиная с 3-х суток, для интактного полушария снижение с 7-х суток становилось достоверным. При этом в группе плацебо индекс 9-ритма незначительно увеличивался к 3-м и 7-м суткам по сравнению с 1-ми. На 14-е сутки соотношение медленной и быстрой активности (М/Б) в группе пациентов, получавших мексидол, было достоверно ниже, чем в группе получавших плацебо (соответственно 1,54 и 2,8; р<0,05) (табл. 3).
Таблица 3. Показатели биоэлектрической активности мозга и их динамика в двух группах больных
Показатель ЭЭГ Сутки Полушарие Плацебо Мексидол Р Ап/Аз 3-и А 1,14±0,31 1,20±0,75 <0,74 Б 1,28±0,48 0,91±0,32 <0,01 7-е А 0,97±0,33 0,86±0,29 <0,38 Б 1,22±0,96 0,74±0,26 <0,11 14-е А 0,96±0,23 0,78±0,32 <0,17 Б 1,05±0,26 0,66±0,14 <0,001 3-1-е А 0,17±0,29 0,07±0,71 <0,57 Б 0,31±0,64 -0,04±0,29 <0,05 7-1-е А 0,01±0,48 -0,26±0,45 <0,14 Б 0,25±0,99 -0,26±0,26 <0,09 14-1-е А -0,21±0,3 -0,31±0,46 <0,61 Б -0,001±0,3 -0,35±0,30 <0,03 Индекс θ-ритма 3-и А 0,09±0,05 0,11±0,06 <0,17 Б 0,09±0,02 0,12±0,06 <0,03 14-е А 0,09±0,04 0,10±0,07 <0,48 Б 0,07±0,03 0,12±0,04 <0,01 7-1-е А -0,02±0,07 -0,02±0,05 <0,98 Б 0,01±0,05 -0,03±0,06 <0,04 14-1-е А -0,06±0,10 -0,001±0,06 <0,07 Б -0,02±0,06 -0,02±0,05 <0,78 М/Б 14-е А 2,7±0,18 1,54±0,33 <0,03 Б 1,19±0,73 0,88±0,58 <0,35 Таким образом, применение мексидола в остром периоде ишемического инсульта в каротидной системе способствует нормализации биоэлектрической активности головного мозга. Тенденция к нормализации зонального распределения α-ритма с 3-х суток и снижение индекса θ-ритма в здоровом полушарии пациентов, получавших мексидол, дополнительно подтверждают влияние этого препарата в первую очередь на структуры подкорково-диэнцефального уровня.
С учетом основных механизмов действия мексидола, показанных в экспериментальных работах [2], был проведен анализ активности ферментов антиоксидантной системы у пациентов обеих групп в сравнении с контролем.
У всех больных в первые дни инсульта выявлялось достоверное снижение активности СОД по сравнению с контролем. На 3-й сутки развития инсульта в группе получавших плацебо определялась более высокая активность этого фермента по сравнению с получавшими мексидол (р<0,01), однако обращают на себя внимание инверсия значений активности СОД к 14-м суткам заболевания и отсутствие достоверных различий с контролем (получавшие мексидол, табл. 4).
Таблица 4. Активность СОД в двух группах больных, ед/НЬ
Группа Сутки инсульта Контроль 1-е 3-й 7-е 14-е Плацебо 215,9±91,5* 224±82,2* ˆ 211,4±70,9** 210,3±82,9** 278,8±66 Мексидол 181,7±95,3** 163,8±94,9** 172,6±90,2** 220,2±94,9 При оценке прироста активности СОД было выявлено ее значительное повышение при назначении мексидола, наиболее выраженное к 14-м суткам заболевания (табл. 5).
Таблица 5. Динамика активности митохонлриальных ферментов, ШФ, ферментов антиоксидантной системы, концентрации TSH и ТБКРП в двух группах больных
Сутки Группа сод, ед/НЬ Каталаза, ммоль/ мин/НЬ ГПС ГР Г-SH, мкмоль/НЬ ТБКРП, нмоль/мл СДГ α-ГФДГ ЩФ мкмоль/мин/НЬ усл.ед. 3-1-е П 8,12 0,07 1,7 0,17* -0,17 0,28 -1,6 26,13 26,13 М -17,96 -0,2 0,3 -0,4 -0,17 0,3 31,67* -4,78 -4,78 7-1-е П -4,42 -0,09 1,0 0,2 0,04 0,4 25,79 42,5 42,5 М -9,17 -0,2 0,9 0,18 -0,09 0,4 20,13 -63,1* -63,1 14-1-е П -5,58 0,18 0,5 0,09 0,8 0,3 -54 34,36 34,36 М 38,48* -0,08 2,9* 0,2 1,04 0,4 -23,6* -54,9* -54,9 Примечание. П - плацебо, М - мексидол. * - достоверные различия между группами (p<0.05).Исследование другого базисного фермента антиоксидантной системы - каталазы выявило достоверное (p<0,01) снижение его активности в 1-е, на 3, 7 и 14-е сутки по сравнению с контролем как в группе получавших плацебо, так и в группе мексидола. При этом достоверных различий в активности фермента между группами пациентов не наблюдалось. В то же время ее прирост претерпевал в группах больных достаточно схожие изменения, что может свидетельствовать об отсутствии влияния мексидола на активность каталазы (см. табл. 5).
Исследование редокс-системы глутатиона выявило достоверное (р<0,01) снижение по сравнению с контролем активности ГПО в обеих исследуемых группах в 1-е, на 3, 7 и 14-е сутки. Как видно из табл. 5, динамика активности этого фермента существенно различалась между группами: значительно повышалась при назначении мексидола, тогда как на фоне применения плацебо снижалась к 14-м суткам заболевания (р<0,05).
Достоверного изменения активности ГР при сравнении групп больных между собой и с контролем выявлено не было, однако зарегистрирован ее значительный прирост у пациентов, получавших мексидол (см. табл. 5).
Анализ динамики содержания Г-SH выявил его достоверное (p<0,01) снижение у пациентов обеих групп в 1-е, на 3 и 7-е сутки инсульта по сравнению с контролем, тогда как на 14-е сутки достоверное снижение содержания Г-SH наблюдалось только в группе получавших мексидол (p<0,01). Тем не менее динамика содержания этого субстрата у пациентов обеих групп была аналогичной (см. табл. 5).
Зафиксированные изменения активности ферментов редокс-системы глутатиона свидетельствуют о выраженности реакций, протекающих с образованием перекисей, а также об их интенсификации на фоне применения мексидола, что, однако, сопровождается усилением восстановления пула Г-SH.
О выраженности процессов окислительного стресса свидетельствует также повышение концентрации ТБКРП. В 1-е, на 3 и 7-е сутки у больных, получавших мексидол, она была достоверно выше контроля (p<0,01), тогда как на 14-е сутки достоверных отличий не отмечено. Динамика содержания ТБКРП в группах больных была достаточно схожей (см. табл. 5).
Учитывая способность мексидола оптимизировать энергосинтезирующие функции митохондрий за счет активации сукцинатоксидазного пути окисления, определяли активность СДГ, α-ГФДГ и ЩФ (см. табл. 5).
У пациентов обеих групп наблюдалась тенденция к снижению активности СДГ с течением инсульта. У получавших плацебо наблюдалось ее достоверное (p<0,05) снижение на 7-е и 14-е сутки развития инсульта по сравнению с контролем, тогда как у пациентов, получавших мексидол, достоверных отличий от контрольных значений не установлено. К 14-м суткам активность этого фермента была достоверно (p<0,05) более высокой на фоне назначения мексидола, чем в группе плацебо.
Активность α-ГФДГ у пациентов обеих групп была достоверно (p<0,05) повышена во все сроки исследования. Однако в группе мексидола зафиксировано ее достоверное (p<0,05) снижение на 7-е и 14-е сутки инсульта.
При корреляционном анализе у пациентов, получавших плацебо, выявлена единственная достоверная ассоциация между активностью СДГ и α-ГФДГ на 3-й сутки инсульта (r=0,5; p<0,05). У пациентов, получавших мексидол, установлены прямые, более сильные, корреляции между активностью СДГ и α-ГФДГ на 3-й и 14-е сутки (r=0,7; p<0,05 и r=0,8; p<0,05), а также обратные между активностью СДГ на 3-й сутки и уровнем ЩФ на 3, 7-и, 14-е сутки (r=-0,8; p<0,05).
Итак, у получавших мексидол пациентов по сравнению с получавшими плацебо происходило нарастание активности СДГ и снижение активности α-ГФДГ и ЩФ.
Повышение активности СДГ, свидетельствующее об активации основного - сукцинатоксидазного метаболического пути получения энергии, характерно для действия мексидола - препарата, являющегося антигипоксантом прямого действия. Снижение активности α-ГФДГ у пациентов, получавших мексидол, по-видимому, является компенсаторным и свидетельствует о снижении анаэробных и усилении аэробных процессов получения энергии. Таким образом, на фоне введения мексидола происходит переход преимущественно анаэробного пути получения энергии на аэробный. Это подтверждается инверсией отношения СДГ к α-ГФДГ, наблюдаемой к 7-м суткам от начала развития инсульта (рис. 3).
Рис.3 Динамика отношения СДГ/α-ГФДГ в двух группах больных.
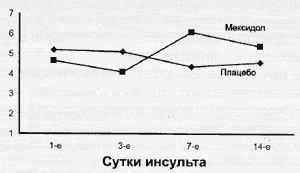
Переход на преимущественно аэробный путь получения энергии за счет активации сукцинатоксидазной метаболической цепи у пациентов, получавших мексидол, приводит к стабилизации клеточных мембран и снижению активности ЩФ, что находит свое отражение в формировании обратной корреляционной связи между активностью СДГ и ЩФ.
Таким образом, в проведенном комплексном исследовании (клиническое, нейрофизиологическое, биохимическое и цитохимическое) установлена достоверная эффективность мексидола в остром периоде ишемического инсульта, наиболее выраженная при его раннем (до 6 ч от начала заболевания) назначении.
Впервые проведенное рандомизированное двойное слепое плацебо-контролируемое исследование эффективности и безопасности мексидола демонстрирует целесообразность введения этого отечественного антиоксиданта-антигипоксанта в комплекс оказания ранней неотложной помощи больным с ишемическим инсультом в каротидной системе атеротромботического или кардиоэмболического патогенетического типа.
Выводы
1. Курсовое введение мексидола (в течение 2 нед от начала развития инсульта) пациентам с ишемическим инсультом в каротидной системе приводит к достоверному (p<0,05) ускорению регресса неврологических нарушений.
2. Раннее (в первые 6 ч инсульта) начало терапии мексидолом достоверно (p<0,05) по сравнению с применением плацебо ускоряет восстановительную динамику и улучшает исход заболевания (p<0,05).
3. Применение мексидола в остром периоде ишемического инсульта в каротидной системе безопасно при соблюдении показаний и противопоказаний к его назначению.
4. Лечение мексидолом больных в остром периоде ишемического инсульта в каротидной системе способствует нормализации биоэлектрической активности головного мозга. Результаты острой фармакологической пробы свидетельствуют о предупреждении им закономерной отрицательной динамики биоэлектрической активности головного мозга в остром периоде заболевания. В то же время в группе плацебо отмечено достоверное увеличение индекса θ-активности (p<0,05), уменьшение частоты α-ритма (p<0,005), увеличение индекса Ап/Аз (p<0,05), увеличение представленности медленной активности по отношению к быстрой (p<0,05).
5. Анализ активности антиоксидантной системы в остром периоде ишемического инсульта позволяет установить достоверное повышение активности СОД (p<0,05) на фоне лечения мексидолом по сравнению с плацебо, а также активацию ферментов следующего звена антиоксидантной системы - ГПО и ГР (p<0,05).
6. Применение мексидола в остром периоде ишемического инсульта приводит к повышению активности СДГ (p<0,05) и снижению активности α-ГФДГ (p<0,05), что свидетельствует об оптимизации работы дыхательной цепи митохондрий, приводящей к стабилизации клеточных мембран и снижению активности ЩФ.ЛИТЕРАТУРА
1. Гусев Е.И., Скворцова В.И. Ишемия головного мозга. М: Медицина 2001.
2. Дюмаев К.М., Воронина Т.А., Смирнов Л.Д. Антиоксиданты в профилактике и терапии патологий ЦНС. M: Из-во Института биомедицинской химии РАМН 1995.
3. Лобшина О.В., Бобахо В.В. Антиоксидантная терапия инсульта на догоспитальном и госпитальном этапах. Материалы научно-практической конференции по неврологии. M 2000.
4. Методические рекомендации по применению антиоксиданта мексидол у больных с острыми нарушениями мозгового кровообращения. М 2000.
5. Одинак М.М., Вознюк И.А. Вестн практ неврол 2003;7:21-26.
6. Скворцова В.И., Раевский К.С, Коваленко А.В. и др. Нейропротективное действие глицина в остром периоде ишемического инсульта. Журн неврол и психиат 1999;99:2:34-39.
7. Методические рекомендации по профилактике и лечению инсульта. Европейская инициативная группа по проблеме инсульта 2003.
| Июнь 2008 г. |