Опубликовано в журнале Терапевтический архив, 2000;72(10):23-27Роль Грандаксина в лечении функциональных заболеваний желудочно-кишечного тракта
М.Ф. Осипенко, Ю.Л. Храмов, ТА Макарова, Е.Г. Вдовенко
Новосибирская государственная медицинская академия, Новосибирский гастроэнтерологический центрВ регуляции функций желудочно-кишечного тракта (ЖКТ) важное место занимает вегетативная нервная система (ВНС) - одно из звеньев, обеспечивающих связь между висцеральными органами и ЦНС. Надсегментарные отделы ВНС ответственны не только за вегетативную регуляцию функций внутренних органов, но и за психоэмоциональное состояние (настроение, двигательную активность, эмоции человека). Именно поэтому различные нарушения деятельности ВНС, в том числе ее надсегментарных отделов, приводят, с одной стороны, к эмоциональным нарушениям, с другой - оказывают неблагоприятное влияние на моторно-эвакуаторную функцию ЖКТ, принимают участие в формировании висцеральной гиперчувствительности [1-3]. Висцеральная гиперчувствительность и моторно-эвакуаторные нарушения являются основными звеньями патогенеза функциональных заболеваний ЖКТ, распространенность которых в популяции велика [4,5]. Около 50% больных, обращающихся за помощью к гастроэнтерологии, страдают различными функциональными заболеваниями пищеварительной системы.
По нашим данным, в целом совпадающим с данными литературы, около 70% больных гастроэнтерологической патологией имеют различные варианты тревожных состояний и нуждаются в их коррекции [6-8]. У больных с патологией ЖКТ часто встречаются ипохондрический и депрессивный синдромы. Помимо основных симптомов у них отмечаются различные проявления вегетативных дисфункций других органов и систем. В большой степени это касается и пациентов с функциональными заболеваниями пищеварительной системы. Одним из часто встречающихся нарушений эмоциональной сферы у больных с гастроэнтерологической патологией являются непсихотические психические расстройства, проявляющиеся различными вариантами неврозоподобной симптоматики [1-9]. Общая их черта - наличие тревоги. Клинически тревога проявляется неосознанным, беспредметным чувством внутреннего напряжения, беспокойством, ожиданием опасности, несчастья, ощущениями беспомощности, неуверенности в себе, бессилия перед внешними факторами, преувеличением их угрожающего характера. Психомоторный компонент ее может быть представлен мимическими явлениями, заторможенностью, оцепенением. Тревога может сопровождаться и выраженным вегетативным компонентом: учащенным дыханием, бессонницей, сухостью во рту, потливостью, диареей, колебаниями АД, тахикардией, потерей или повышением аппетита, снижением либидо и потенции, гипервентиляцией и др.
Для коррекции этих нарушений, которые могут быть проявлением личностных особенностей и провоцировать появление симптомов со стороны висцеральных органов или, наоборот, могут быть обусловлены соматической патологией, необходим комплексный подход [1-9]. Терапия, направленная на купирование исключительно гастроэнтерологических симптомов, не всегда дает желаемый результат, поскольку не полностью корректирует эмоциональные и вегетативные нарушения, являющиеся звеньями патогенеза. Среди медикаментозных препаратов, применяемых с целью нормализации эмоциональных и вегетативных нарушений, используют антидепрессанты и транквилизаторы в малых дозах. Среди транквилизаторов ведущее положение занимают бензодиазепины благодаря своему анксиолитическому, седативному, миорелаксирующему и антиконвульсивному действию. Но препараты этой группы зачастую вызывают дневную сонливость, слабость, снижение трудоспособности, усиливают явления мышечной слабости.
Одним из анксиолитиков, относящихся к бензодиазепинам, но имеющим атипичное строение, является Грандаксин [2,10]. Из-за своего нетипичного химического строения он не обладает гипнотическим свойством, не вызывает миорелаксации, не является антиконвульсантом, не потенцирует действие алкоголя, не нарушает координацию. Грандаксин улучшает психомоторную и интеллектуальную функции, оказывает слабое психостимулирующее действие (улучшает логическую память, вербальную аргументацию, психическую производительность) и потому позволяет вести больным активный образ жизни.
Целью исследования была оценка эффективности Грандаксина в коррекции эмоциональных и вегетативных нарушений, а также клинических синдромов у пациентов с функциональной патологией ЖКТ.
Материал и методы
Были отобраны 59 пациентов (24 мужчины и 35 женщин в возрасте от 18 до 65 лет, средний возраст 45,3±1,41 года), имеющих различные функциональные заболевания пищеварительной системы, подтвержденные при детальном обследовании, у которых были также диагностированы выраженные психовегетативные нарушения и отсутствовал достаточный эффект от стандартной целенаправленной терапии на амбулаторном этапе лечения.Больных разделили на 3 категории в зависимости от преимущественной локализации функциональных нарушений. 16 пациентов имели симптомокомплекс билиарной диспепсии в результате дискинезии желчевыводящих путей (ЖВП) без признаков их органического поражения. 15 больных с патологией верхних дыхательных отделов ЖКТ беспокоили проявления функциональной диспепсии. Категория пациентов с патологией кишечника была представлена 28 больными с синдромом раздраженной кишки. Больные основной группы - ОГ (43 человека) и группы сравнения - ГС (16 человек) в зависимости от основных клинических проявлений получали желчегонные и спазмолитики при явлениях билиарной диспепсии; антациды, ингибиторы кислотности и прокинетики- при функциональной диспепсии и прокинетики и селективные антагонисты кальция при синдроме раздраженной кишки. Больные ОГ помимо вышеуказанного лечения принимали Грандаксин по 50 мг 3 раза в день. Пациенты ГС получали симптоматическое лечение, им не назначали терапию, целенаправленно влияющую на вегетативно-эмоциональные нарушения. Длительность стационарного лечения составила 14 дней.
Психоэмоциональное состояние оценивали по шкале самооценки (анкета Спилбергера-Ханина) до и после лечения. Балльный анализ полученных результатов позволял судить о коэффициенте тревожности по следующей формуле: Т=Р-О-50, где Р - сумма баллов строк 3, 4, 6, 7, 9, 12,13, 14,17, 18; 0 - сумма баллов строк 1, 2, 5, 8, 10, 11, 15, 16,19, 20; Т - коэффициент тревожности. Значения коэффициента тревожности расценивали следующим образом: ниже 41 балла - низкая тревожность, 41-45 баллов - умеренная тревожность, 46 баллов и выше - высокая.
Состояние ВНС оценивали по двум анкетам, предложенным в монографии A.M. Вейна [1]. Первая позволяла выявить признаки вегетативных нарушений и оценить их динамику в процессе лечения (балльная система). При наличии 25 баллов и более можно говорить о синдроме вегетативной дисфункции. Вторая анкета позволяла определить вегетативный индекс и по нему - преобладающий тип регуляции (симпатический или парасимпатический). В ней учитывали состояние потовых желез, кожи, глазные симптомы, аппетит, состояние сердечно-сосудистой, дыхательной, мочевыделительной, пищеварительной систем, сексуальной сферы, эмоциональное состояние, показатели крови и т.д.
Динамику субъективных ощущений, характерных для функциональной патологии, оценивали за время лечения следующим образом: полное исчезновение симптомов, улучшение, отсутствие динамики, отрицательная динамика.
Статистическую обработку полученных результатов проводили с применением t-критерия Стьюдента, а также с помощью широко используемого в зарубежной литературе показателя OR (отношение шансов) с доверительным интервалом (CI) 95%. OR определяется как отношение шансов события в одной группе к шансам события в другой группе или как отношение шансов того, что событие произойдет, к шансам того, что событие не произойдет; он показывает силу связи между воздействием и результатом. Полное отсутствие эффекта от лечения характеризуется OR=1. Если величина 1 лежит за пределами 95% доверительного интервала наблюдаемого эффекта, то результаты, скорее всего, статистически значимы при уровне значимости 0,05 [11]. В качестве критерия наличия связи между качественными показателями - изменением уровня тревожности и динамикой субъективных ощущений - использовали коэффициент сопряженности Пирсона.
Результаты и обсуждения
Поводом для госпитализации отобранных нами 59 больных с функциональными заболеваниями ЖКТ различной локализации послужили выраженные эмоционально-вегетативные нарушения и отсутствие достаточного эффекта от традиционной симптоматической терапии в амбулаторных условиях. Анкета Спилбергера-Ханина позволяла выявить ситуационную тревожность, уровень которой, оцениваемый в баллах, не различался в ОГ и ГС перед началом стационарного лечения. Эти результаты соответствуют большинству данных литературы, свидетельствующих о высоком уровне тревожности у пациентов с функциональной патологией пищеварительной системы [6,8]. Во всяком случае, это касается лиц, обращающихся за медицинской помощью. При лечении выявлена отчетливая положительная динамика уровня тревожности за 2 недели приема Грандаксина. У 90,7% (39 из 43) больных коэффициент тревожности снизился до низкого или умеренного уровня. В ГС положительная динамика уровня тревожности (до умеренной или низкой) отмечалась у 43,7% (у 7 из 16) больных (OR 2,075; C11,25-2,95).Результаты, отражающие динамику коэффицента тревожности, представлены на рис. 1.
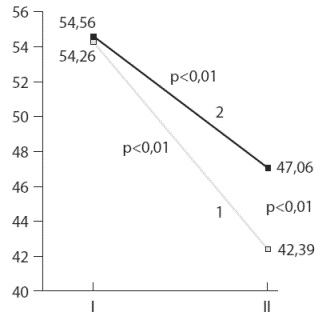
Рис. 1. Изменение коэффициента тревожности у больных с функциональной патологией ЖКТ в процессе лечения
По оси ординат - коэффициент тревожности (в баллах).
1 - ОГ, 2 - ГС. I - начало терапии, II - через 2 нед терапииДо лечения у всех больных ОГ и ГС был высокий уровень тревожности (выше 46 баллов). После лечения он снизился (различия статистически значимы) в ОГ с 54,26±0,6 до 42,39±0,4 балла и менее значительно в ГС - с 54,56±0,86 до 47,06±1,32 балла. В среднем в ОГ коэффициент тревожности уменьшился более значительно, чем в ГС (с высокого до умеренного уровня). Определенный эффект в снижении уровня тревожности был связан с использованием при лечении препаратов гастроэнтерологического профиля, бесед с лечащим врачом, разъясняющим функциональный характер патологии, а также с эффектом Хауторна [11], заключающимся в изменении характера поведения пациентов, являющихся предметом особого наблюдения и интереса, в их стремлении "порадовать доктора", внести вклад в получение хороших результатов. Но существенно более значительное снижение уровня тревожности в ОГ, чем в ГС, свидетельствует о высокой эффективности Грандаксина как анксиолитического средства при функциональной патологии ЖКТ.
Существенных различий в динамике уровня тревожности в зависимости от локализации патологического процесса в ЖКТ не выявлено (табл.1).
Таблица 1. Динамика коэффициента тревожности при различных функциональных заболеваниях ЖКТ в процессе лечения
Патология ЖКТ Коэффициент тревожности p1 p2 до лечения после лечения Функциональная диспепсия: ОГ (n=10) 53,90+1,59 42,30+0,71 <0,01 <0,05 ГС (n=5) 53,89+1,17 49.20+3,34 >0,05 Дискинезии ЖВП: OГ (n=11) 52,54+1,43 41,54+0,41 <0,01 <0,01 ГС (n=5) 54,33+1,58 45,83+1,72 <0,05 Синдром раздраженной кишки: ОГ (n=22) 55,50+0,62 43,23+0,62 <0,01 <0,01 ГС (n=6) 57,20+0,58 47,60+1,17 >0,05 Здесь и в табл. 2: p1 - достоверность различий до и после лечения, p2-достоверность различий между ОГ и ГС после лечения
Обращает на себя внимание лишь несколько более высокий коэффициент тревожности у больных с синдромом раздраженной кишки (как исходный, так и после лечения), что в основном соответствует данным других исследований [9]. Поскольку его снижение до низких значений не произошло за 2 недели лечения ни в одной из групп, вероятно, необходим более длительный курс терапии Грандаксином.
Таким образом, Грандаксин показал себя хорошим средством коррекции синдрома тревожности у больных с функциональной патологией ЖКТ независимо от локализации патологического процесса.
Одновременно с психоэмоциональным состоянием в процессе терапии оценивали выраженность вегетативной дисфункции по двум шкалам, предложенным A.M. Вейном [1]. Перед лечением она была выявлена у всех наших пациентов. У 19 из 59 обследованных исходно преобладала симпатическая регуляция, у 22 - парасимпатическая, у 18 не отмечалось явного преобладания влияния того или другого отдела ВНС. В ОГ положительный результат (уменьшение выраженности вегетативной дисфункции) отмечен у 38 (88,4%) из 43 пациентов, а в ГС - у 6 (37,5%) из 16 (OR 2,36; 95% Cl 1,08-3,04). У 41,9% больных ОГ проявления вегетативной дисфункции, согласно балльной системе оценки, не определялись после 2 недель лечения, в ГС - только у 18,7% (OR 2,19; 95% CI 1,02-3,14). Выраженность вегетативных нарушений в ОГ уменьшилась с 39,91 ±0,59 до 27,77±0,93 балла, а в ГС - с 39,93±0,87 до 31,93±1,39 балла (рис.2).
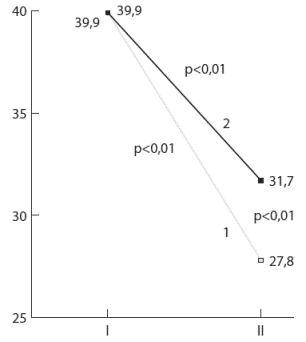
Рис. 2. Изменение выраженности вегетативной дисфункции у больных с функциональной патологией ЖКТ в процессе лечения
По оси ординат - вегетативная дисфункция (в баллах).
Остальные обозначения те же, что и на рис. 1Из табл. 2 видна отчетливая положительная динамика состояния ВНС у больных с различной патологией ЖКТ, наиболее заметная при включении в комплексное лечение анксиолитика Грандаксина.
Таблица 2. Динамика вегетативной дисфункции при различной функциональной патологии ЖКТ в процессе лечения
Патология ЖКТ Вегетативная дисфункция, баллы p1 p2 до лечения после лечения Функциональная диспепсия: ОГ (n=10) 37,9+1,06 24,7+0,97 <0,01 <0,01 ГС (n=5) 37,8+1,69 30,0+2,0 <0,05 Дискинезии ЖВП: ОГ (n=11) 38,37+0,99 23,18+0,85 <0,01 <0,05 ГС (n=5) 39,4+1,43 30,2+3,26 <0,05 Синдром раздраженной кишки: ОГ (n=22) 41,31+0,80 31,27+1,30 <0,01 >0,05 ГС (n=6) 41,33+1,67 33,0+1,53 <0,01 Примечание: вегетативную дисфункцию констатируют при 25 баллах и более
Наиболее значимые изменения произошли у больных с функциональной патологией верхних отделов ЖКТ и ЖВП. Необходимо отметить, что в ГС, в которой не проводили целенаправленного воздействия на ВНС и ЦНС, отмечалась положительная динамика. Можно предположить, что эти изменения отражают обратную связь между висцеральными органами и надсегментарными отделами ВНС. Поэтому улучшение функционирования органов ЖКТ приводит к уменьшению проявлений вегетативной дистонии других систем и органов. Преобладание вегетативного тонуса достоверного влияния на эффект лечения не оказывало.
Таким образом, включение в комплексное лечение функциональных заболеваний Грандаксина благоприятно сказалось на состоянии ВНС и уменьшило выраженность ее дисфункций. В ОС и ГС в целом отмечалось улучшение состояния больных. Выявлена тесная корреляционная связь между снижением коэффициента тревожности и динамикой гастроэнтерологических симптомов. Так, коэффициент сопряженности Пирсона был равен 0,532, что свидетельствует о тесной связи между данными явлениями.
Таким образом, снижение уровня тревожности и выраженности вегетативных нарушений сопровождается уменьшением выраженности клинических проявлений нарушения функций пищеварительной системы. Это подтверждает роль ВНС и ЦНС в регуляции функций ЖКТ и участие эмоциональных и вегетативных нарушений в патогенезе функциональных заболеваний пищеварительной системы [12-14].
Для более подробного анализа влияния Грандаксина на функцию ЖКТ у 18 пациентов из ОГ подробно анализировали скорость транзита по толстой кишке с помощью карболенового теста. Основными клиническими проявлениями у этих больных явились нарушения пассажа из-за наличия синдрома раздраженной кишки на фоне аномалий строения и положения толстой кишки (мегаколон, долихоколон, синдром Хилаидити, колоноптоз), у них отсутствовал достаточный эффект от терапии цизапридом и селективными антагонистами кальция на догоспитальном этапе. Поэтому они были включены в ОГ и на этапе стационарного лечения им был добавлен Грандаксин (по 50 мг 3 раза в день). Оценивали его эффект на скорость пассажа по толстой кишке после 2 недель лечения. У 83,3% больных получен положительный эффект (рис. 3).
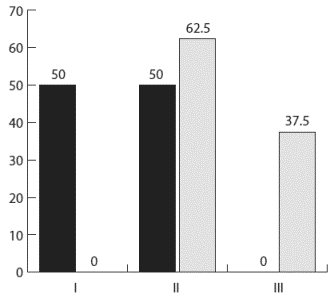
Рис. 3. Результаты добавления Грандаксина к лечению больных с синдромом раздраженной кишки
По оси ординат - % больных
Светлые столбики - замедленный транзит.
I - нормализация, II - улучшение, III - без динамикиНаиболее значимым он был у пациентов с ускоренным пассажем. Так, у всех 10 больных с ускоренным пассажем отмечалось улучшение при добавлении к лечению Грандаксина, а в 50% случаев констатирована нормализация пассажа. При замедлении транзита положительный эффект отмечался лишь у 5 (62,5%) пациентов из 8, а у 3 больных эффект отсутствовал.
Побочные действия, в том числе характерные для типичных бензодиазепинов и антидепрессантов (сонливость, головокружение, сухость во рту, запоры, повышенное беспокойство, агрессия), в процессе лечения Грандаксином не наблюдались.
Выводы
- Эффективным средством коррекции синдрома тревожности и вегетативных дисфункций у больных с функциональными заболеваниями желудочно-кишечного тракта является Грандаксин.
- Нетипичный бензодиазепин тофизопам (Грандаксин) оказывает положительное влияние на скорость транзита по кишечнику у больных с синдромом раздраженной кишки, особенно при ускоренном пассаже.
- Клинические проявления функциональных заболеваний желудочно-кишечного тракта находятся в тесной корреляционной связи с выраженностью синдрома тревоги.
- Грандаксин хорошо переносится больными и практически не дает побочных эффектов.
Литература
1. Вейн A.M. (ред.) Вегетативные расстройства: клиника, лечение, диагностика. М.: Мед. информ. агентство; 1998.
2. Aggarwai A, Cutts Т, Abe I i Т. Predominant symptoms in irritable bowel syndrome correlate with specific autonomic nervous system abnormalities. Gastroenterology 1994;106:945-950.
3. Camilleri M, Ford M. Functional gastrointestinal disease and the autonomic nervous system: a way ahead? Ibid. 1114-1118.
4. Bueno L. Brain-gut mechanisms of visceral motor activity. In: Corazziari E, ed. Neurogastoenterology. Berlin, New York; de Gruyter; 1996:1-17.
5. Houghton L.A. Sensory dysfunction and the irritable bowel syndrome. Baillieres Best Pract. Res. Clin. Gastroenterol. 1999;13:415-427.
6. Addolorato G. et al. Anxiety and depression: a common feature of health care seeking patients with irritable bowel syndrome and food allergy. Hepato-Gastroenterology; 1998;45:1559-1564.
7. Gwee K.A. et. al. The role of psyhological and biological factors in postinfective gut dysfunction. Gut 1999;44:400-406.
8. Weber J, Denis P. Psychosocial profile of patients with irritable bowel syndrome. In: Denis P., ed. Irritable bowel syndrome. Berlin. New York: de Gruyter; 1995:13-19.
9. Александровский Ю.А., Аведисова A.C., Павлова M.C. О вегетотропном эффекте Грандаксина при лечении невротических расстройств в общесоматической практике. Тер. арх. 1998;10:76-78.
10. Horvath E.J. Anxiolytic 2,3-benzodiazepines, their spesific binding to the basal ganglia. Progr. Neurobiol. 2000;60:309-342.
11. Флетчер P., Флетчер С, Вагнер Э. Клиническая эпидемиология. Основы доказательной медицины. М.: Медиа Сфера: 1998.
12. Bharucha A, Camilleri М, Low P. Autonomic dysfunction in gastrointestinal motility disorders. Gut. 1993;34:397-401.
13. Hausken T. Common pathogenetic mechanisms in symptomatic, uncomplicated gallstone disease and functional dyspepsia: volume measurement of gallbladder and antrum using threedimensional ultrasonography. Dig. Dis. Sci. 1997;42:2505-2512.
14. Malagelada J.R. Disturbed upper gastrointestinal sensation: an important abnormality? Aliment. Pharmacol. Ther. 1997;11 (suppl. 2):51-56.
| Май 2014 г. |