Опубликовано в:
«CONSILIUM MEDICUM» »»
Лекарственное лечение при распространенном первичном раке печени
В.В.Бредер, к.м.н., старший научный сотрудник отделения химиотерапии ГУ РОНЦ им. Н.Н.Блохина
РАМН, Москва
1. Накопленный к настоящему времени опыт химиотерапии при ГЦР позволяет говорить о том, что при данном заболевании лекарственная терапия возможна только у очень небольшой группы больных (отсутствие цирроза, низкий уровень билирубина), хотя на показатели выживаемости это существенно не влияет. В последнее время определенные перспективы лекарственной терапии ГЦР связаны с появлением препарата Нексавар (сорафениб), зарегистрированным изначально для лечения метастатического почечно-клеточного рака, а в сентябре 2008 г. - и для лечения ГЦР. Механизм его действия связан с блокированием пролиферации опухолевой клетки и ангиогенеза за счет блокирования рецепторов, связанных с неоангиогенезом. Ни один из других известных и доступных для исследований II и III фазы препаратов такими свойствами не обладает.
1. Сорафениб блокирует как пролиферацию опухолевой клетки, так и ангиогенез (in vitro)
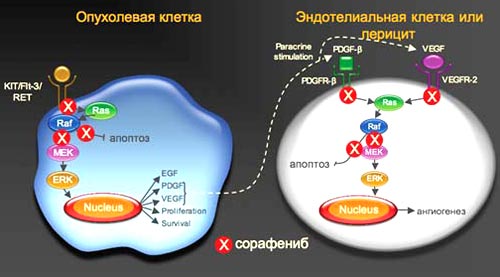
Wilhelm 5W et al Cancer Res 2004: 64: 7099-109.
2. Исследование SHARP было направлено на выяснение возможностей лекарственного лечения ГЦР с помощью сорафениба. Исследование проводилось на достаточно большой группе больных (n=602), не получавших предварительно системной терапии, критерии включения в исследование характерны для достаточно благоприятного течения заболевания. Сравнение проводилось с группой плацебо, что вполне оправданно при опухоли, рефрактерной к лекарственной терапии. Первичной конечной точкой в исследовании были выживаемость и время до симптомного прогрессирования, вторичной - время до прогрессирования.
2. Исследование SHARP: сорафениб при распространенном неоперабельном ГЦР
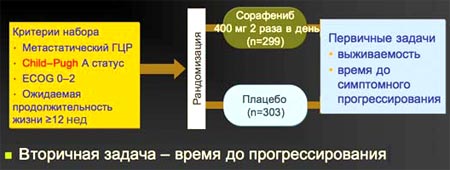
ECOG PS - Eastern Cooperative Oncology
Group Performance SlatusUovsr JM et al N Engl J Med. 2008 Jul 24: 359(4): 378-90.
3. Кривые времени до прогрессирования достоверно расходятся однозначно в пользу сорафениба с медианой времени до прогрессирования в исследуемой группе 24 нед, тогда как для группы плацебо этот показатель составил 12,3 нед. Наблюдалось увеличение времени до прогрессирования на 73%, разница была статистически достоверна.
3. SHARP: время до прогрессирования
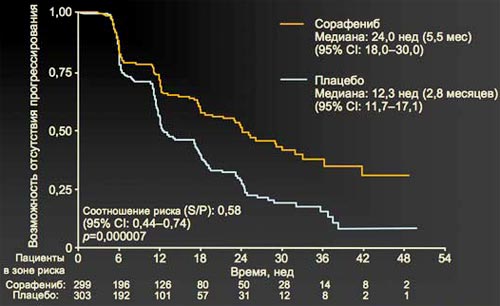
Liovsr JM et al. N Engl J Med. 2008 Jul 24: 359(4): 378-90
4. Возможно, разница в общей выживаемости не кажется такой значительной, но это первое рандомизированное исследование, показавшее статистически достоверное увеличение выживаемости больных с ГЦР на фоне лекарственной терапии. Прирост общей выживаемости составил 44%.
4. SHARP: общая выживаемость
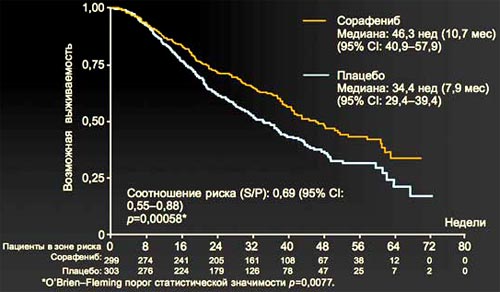
Liovet JM et al. N Engl J Med. 2008 Jul 24; 359(4): 378-90.
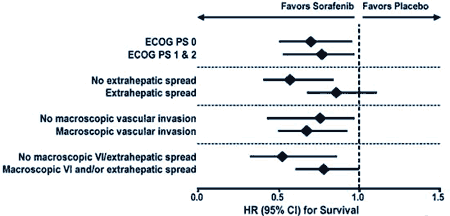
5. Кого можно лечить и на какие факторы прогноза можно рассчитывать при назначении сорафениба больным с ГЦР? Для ответа на этот вопрос было проведено исследование эффективности в подгруппах, показавшее его эффективность как у больных с удовлетворительным состоянием, так и у больных с симптомными проявлениями заболевания, как при отсутствии внепеченочных метастазов, так и при их наличии, с макроскопической инвазией сосудов и при ее отсутствии.
5. SHARP: анализ эффективности в подгруппах
6. Изучение профиля безопасности сорафениба продемонстрировало хорошую переносимость препарата - было показано отсутствие достоверных различий частоты нежелательных побочных реакций. В I и II фазе клинических исследований была отработана доза - считается, что клинически эффективной является доза 800 мг/сут, разделенная на 2 приема. Тем не менее, не всеми пациентами указанная доза переносится хорошо. Пациентов с ГЦР стадии Child B и с компрометированной функцией печени (т.е. с признаками гепатолиза, холестаза) можно лечить сорафенибом, но гораздо более аккуратно и при первом появлении признаков токсичности очень важно вовремя перейти на уменьшенную дозу - по современным рекомендациям сразу делается перевод на дозу 400 мг, также разделенную на 2 приема. Для сорафениба, как для любого таргетного препарата из группы мультикиназных ингибиторов, характерна ранняя токсичность в виде кожной сыпи, ощущения плохого самочувствия; эти проявления проходят самостоятельно без редукции дозы через 2-3 нед.
6. SHARP: сорафениб – благоприятный профиль токсичности
Сорафениб
(n=297)Плацебо
(n=302)Лечение серьезных побочных
явлений (SAE, %)52 54 Аллергический реакции, % 13 9 Побочные эффекты, % All Gr 3/4 All Gr3/4 Диарея 39 8/- 11 2/- Боль в животе 8 2/- 3 <1/- Потеря массы тела 9 2/- <1 0/- Анорексия 14 <1/- 3 <1/- Тошнота 11 <1/- 8 1/- Ладонно-подошвенный синдром 21 8/- 3 <1/- Рвота 5 1/- 3 <1/- Алопеция 14 0/- 2 0/- Гепатотоксичность <1 <1/- 0 0/- Кровотечения 7 <1/- 4 <1/<1 Uovet JM et al. N Engl J Med. 200B Jul 24; 359(4): 378-90.
7. Подобные результаты были получены в аналогичном рандомизированном плацебо-контролируемом исследовании, проведенном в Азиатско-Тихоокеанском регионе. Несколько отличающиеся значения медианы выживаемости связаны с тем, что в это исследование вошло гораздо больше больных с плохим прогнозом (цирроз печени на фоне гепатита В и нарушение функции печени - Child-Pugh B ). Сейчас можно сказать, что у нас есть единственный препарат - Нексавар, назначая который больным неоперабельным ГЦР, можно рассчитывать на увеличение продолжительности жизни (уровень доказательности А).
7. Рандомизированное исследование III фазы сорафениб vs плацебо при распространенном ГЦР у пациентов, проживающих в АТР (Азиатско-Тихоокеанском регионе)
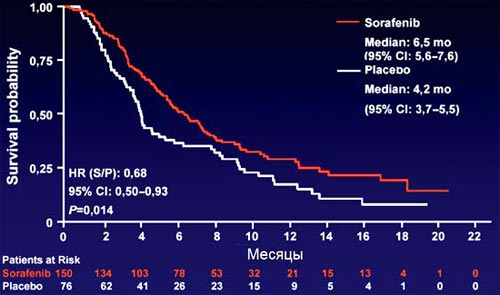
Cheng A et al J Clin Ortcof. 2000:26. Abstract 4509. Updated from oral presentation at ASCO; Chicago. IL: June 2008.
8. У нашего отделения есть некоторый опыт применения Нексавара, и в связи с этим появился ряд вопросов. Одним из таких вопросов является определение показаний к его использованию. Мы считаем, что Нексавар можно применять при ГЦР у достаточно сохранных больных, при этом больным с Child A и B показано применение Нексавара, а при стадии Child С целесообразность его применения остается под большим вопросом. Мы считаем, что в тех случаях, когда хирурги сомневаются в радикальности проведенной операции, есть смысл назначить Нексавар, а также в сочетании с абляцией и химиоэмболизацией. Сейчас также изучается возможность применения препарата в качестве адьювантной терапии.
8. Кого и когда лечить?
- Гепатоцеллюлярный рак
- Объективный статус B03=0-2
- Child-Pugh А, В (С?)
- Местно-распространенный и диссеминированный
- Прогрессирование процесса после локального лечения или невозможности его проведения
- В сочетании с паллиативным локальным лечением, после разрешения осложнений
- условно-радикальной резекции
- абляции
- (химио)эмболизации
- Адъювантное лечение???
9. Много внимания в последнее время уделяется изучению возможности комбинации сорафениба с другими препаратами. В рандомизированное исследование II фазы, опубликованное в 2008 г., было включено 96 больных, рандомизированных на две равные группы: доксорубицин+сорафениб и доксорубицин + плацебо. Исследование продемонстрировало достоверные различия общей выживаемости в пользу комбинированной терапии: общая выживаемость 13,7 мес против 6,5 мес. Данная комбинация может рассматриваться как возможный вариант нового стандарта лечения больных ГЦР. Также возможным перспективным направлением, которое будет разрабатываться, является комбинация сорафениба с бевацизумабом, которая сейчас активно изучается. Таким образом, Нексавар - это первый препарат системной терапии, который достоверно увеличивает выживаемость пациентов ГЦР vs плацебо по результатам 2 рандомизированных исследований III фазы в 2 различных популяциях. Показано, что Нексавар проявляет умеренную, предсказуемую и управляемую токсичность. Препарат продемонстрировал дополнительную эффективность в сочетании с доксорубицином при более выраженной токсичности (II фаза) у больных с распространенным ГЦК. Полагаю, что именно комбинированный вариант лечения больных с диссеминированным ГЦР будет наиболее перспективным и успешным.
9.Доксорубицин + сорафениб при ГЦР (II фаза): общая выживаемость
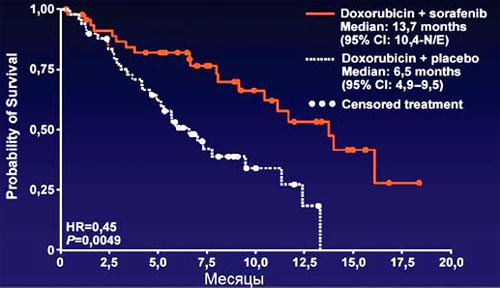
Abou-Alfa GК et al. Eur J Cancer Suppl. 2007; 5(4) -259
добввлено из абстр 128, ASCO-GI; Orlando, FL; January 2008
Материал предоставлен компанией ЗАО «БАЙЕР». Контактная информация:
ЗАО "БАЙЕР"
107113, Москва, 3-я Рыбинская ул., дом 18, строение 2.
Телефон: (495) 231-12-00
Факс: (495) 231-12-02
Компания ЗАО «БАЙЕР» заботится о высоком качестве своей продукции и поэтому заинтересована в получении любой информации по безопасности на продукцию компании в целях дальнейшей оценки и снижения риска возникновения нежелательных реакций у пациентов.
Если Вы хотите сообщить о нежелательном явлении или жалобе на качество продукции компании «ЗАО БАЙЕР», пожалуйста передайте информацию своему лечащему врачу, в регуляторные органы, или воспользуйтесь
| Март 2012 г. |